题目内容
实验室用加热氯酸钾和二氧化锰的混合物制取1.5摩尔氧气.
求:需氯酸钾多少摩尔?质量为多少克?(根据化学方程式列式计算)
求:需氯酸钾多少摩尔?质量为多少克?(根据化学方程式列式计算)
分析:根据氯酸钾在有催化剂和加热的条件下,生成氯化钾和氧气,要注意配平.然后根据氧气的物质的量求出氯酸钾物质的量以及质量即可.
解答:设:需氯酸钾的物质的量为x.
2KClO3
2KCl+3O2↑
2 3
x 1.5mol
=
x=1mol
氯酸钾的质量=1mol×122.5g/mol=122.5g
答:需氯酸钾为1mol,质量为122.5g.
2KClO3
| ||
| △ |
2 3
x 1.5mol
| 2 |
| x |
| 3 |
| 1.5mol |
x=1mol
氯酸钾的质量=1mol×122.5g/mol=122.5g
答:需氯酸钾为1mol,质量为122.5g.
点评:本考点考查了根据化学方程式的计算,是比较基础的计算题,属于已知生成物的质量,求反应物的质量.做题时要注意:化学方程式的书写要正确,否则数据就会出现错误,始终不要忘记质量守恒定律,本考点主要出现在计算题中.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目


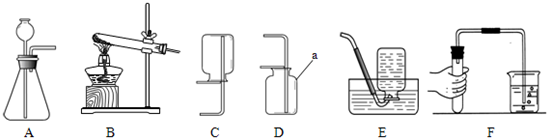
 如图是小华同学用高锰酸钾制取氧气的实验装置图.
如图是小华同学用高锰酸钾制取氧气的实验装置图.
