题目内容
【题目】回答下列问题:
(1)按如图装置对质量守恒定律进行实验探究,观察到反应后天平不平衡质量守恒定律(填“符合”或“不符合”). 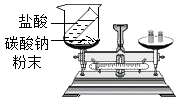
(2)由质量守恒定律可知,化学反应前后,一定不变的是(填序号)
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类
(3)硝酸在工业生产中有广泛的应用,工业上制取硝酸的关键反应为:4NH3+5O2 ![]() 4NO+R,其中R化学式为
4NO+R,其中R化学式为
【答案】
(1)符合
(2)①②⑤
(3)H2O
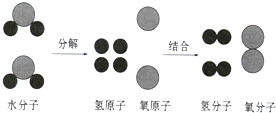
【解析】解:(1)一切化学反应都遵循质量守恒定律,反应后天平不平衡,是因为碳酸钠和盐酸反应生成的二氧化碳逸散到了空气中.(2)化学反应的实质是分子分成原子,原子再重新组合成新的分子,所以反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化,元素的种类、元素的质量、物质的总质量都不变.在此过程中,分子的种类发生了改变,由分子构成的物质的种类也发生了改变;分子数目可能增加也可能减少,也可能前后相等.故化学反应前后一定不变的是①②⑤.(3)在反应4NH3+5O2 ![]() 4NO+6R中,根据质量守恒定律可知,反应前后元素的种类、原子的种类、个数不变,氮原子的个数前后相等,反应前共12个氢原子、10个氧原子,则反应后应共12个氢原子、10个氧原子,反应后已经有4个氧原子,则6R中含有12个氢原子、6个氧原子,又R的化学计量数为6,则R的化学式为H2O.
4NO+6R中,根据质量守恒定律可知,反应前后元素的种类、原子的种类、个数不变,氮原子的个数前后相等,反应前共12个氢原子、10个氧原子,则反应后应共12个氢原子、10个氧原子,反应后已经有4个氧原子,则6R中含有12个氢原子、6个氧原子,又R的化学计量数为6,则R的化学式为H2O.
故答案为:(1)符合; (2)①②⑤;(3)H2O.
(1)天平不平衡是由于反应后生成了气体二氧化碳逸散到空气中,并不是不遵守质量守恒定律.(2)化学变化是分子分成原子,原子再重新结合成新的分子的过程,据此进行分析解答即可.(3)根据化学反应方程式,利用质量守恒定律来推断化学式.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目