��Ŀ����
����Ŀ������һ��ѧ��ѧ��ȤС������ʵ����ʺ���ɽ������̽����
��1������ͬѧ������ͭ��������̼������ͼ1��ʾװ���ڸ��������������½���ʵ�飬������������ijɷֽ���̽����
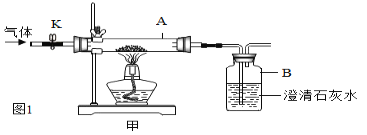
��������⣩���ɵ��������Ƿ���һ����̼��
���û�ѧ����ʽ��ʾ�����������п�����һ����̼�����ɣ�_____��
��ʵ�������ۣ�
����K������ͨ�����ĵ���һ��ʱ�䡣
���ر�K��������һ���¶�ʹ֮��Ӧ
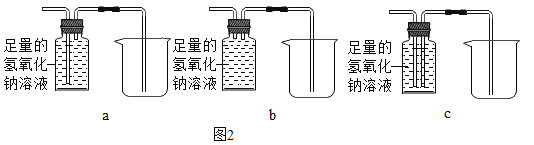
������ͬѧ��������ɵ������еĶ�����̼������ʣ�������ռ��ڼ���ƿ�У�����װ������Ϊ��������_____������ţ���
��ʵ����֤��
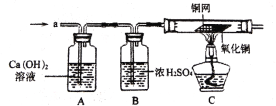
Ϊ�˼������ɵ������к���CO�����ռ��ڼ���ƿ�е������ų�����ͨ��ͼ����ʾ��װ�ý���ʵ�飬A�еĹ������������ͭ��B����Һ��Ϊ����ʯ��ˮ����A������Ϊ_____��B�г���ʯ��ˮ����ǣ���˵��������Ʒ�к���һ����̼��
��ʵ�鷴˼��
̼�ۻ�ԭ����ͭ��ʵ���У������ɵ������к���һ����̼����Ӧʱ����̼������ͭ������֮��_____������ڡ��������ڡ���С�ڡ���3��40
��2������ͬѧ�ⶨˮ���⡢��Ԫ�ص������ȣ���֪��H 2+CuO![]() Cu+H2O��
Cu+H2O��
������ͼ3����ʵ�飬��Ӧ����A�в����ܣ���ҩƷ����������ag��B��U�ιܣ���ҩƷ����������bg��
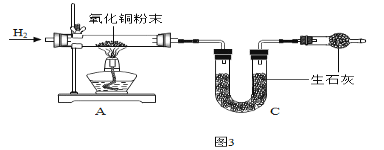
��ˮ���⡢��Ԫ�ص���������_____���ú�a��b��ʽ�ӱ�ʾ����
�����������У��Բⶨ�����Ӱ�����_____������ţ���
A CuO��ĩ������ B CuOû����ȫת��ΪCu C û��Cװ��
���𰸡�C+CO2![]() 2CO c ��ɫ������ɫ ���� ��b��a����a AC
2CO c ��ɫ������ɫ ���� ��b��a����a AC
��������
������⣺
���������£�����ͭ��̼��Ӧ����ͭ�Ͷ�����̼��������̼��̼��Ӧ����һ����̼����Ӧ�Ļ�ѧ����ʽΪ��C+CO2![]() 2CO��
2CO��
ʵ�������ۣ�
�۶�����̼�����������Ʒ�Ӧ����̼���ƺ�ˮ��һ����̼������ˮ�������������Ʒ�Ӧ���ܶȱ�ˮС������ͬѧ��������ɵ������еĶ�����̼������ʣ�������ռ��ڼ���ƿ�У�����װ������Ϊ��������c��
ʵ����֤��
��A�к�ɫ������ɫ��B�г���ʯ��ˮ����ǣ�����Ϊ����ͭ��һ����̼��Ӧ����ͭ�Ͷ�����̼����˵��������Ʒ�к���һ����̼��
ʵ�鷴˼��
̼������ͭ��Ӧ�Ļ�ѧ����ʽΪ��2CuO+C![]() 2Cu+CO2����ÿ160������������ͭ��12������̼ǡ����ȫ��Ӧ��̼������ͭǰ����ȫ��Ӧʱ��������3��40�����ɵĶ�����̼��̼��Ӧ����һ����̼����˷�Ӧʱ����̼������ͭ������֮�ȴ���3��40��
2Cu+CO2����ÿ160������������ͭ��12������̼ǡ����ȫ��Ӧ��̼������ͭǰ����ȫ��Ӧʱ��������3��40�����ɵĶ�����̼��̼��Ӧ����һ����̼����˷�Ӧʱ����̼������ͭ������֮�ȴ���3��40��
��2����Ӧ����A�в����ܣ���ҩƷ����������ag��˵����Ӧ������ͭ����Ԫ��������ag��B��U�ιܣ���ҩƷ����������bg��˵�����ɵ�ˮ��������bg��
��ˮ���⡢��Ԫ�ص��������ǣ�bg��ag����ag����b��a����a��
��A CuO��ĩ��������²ⶨˮ������ƫ�Ӷ����²ⶨ���ƫ��
B CuOû����ȫת��ΪCu����Ӱ��ⶨ�����
C û��Cװ�ã������е�ˮ�����ᱻ��ʯ�����գ����²ⶨˮ������ƫ�Ӷ����²ⶨ���ƫ��ѡAC��

 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д� �����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д�
�����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д� �����ҵ�����������ѧ���ӳ�����ϵ�д�
�����ҵ�����������ѧ���ӳ�����ϵ�д� ����ѧ��Ӯ�����ϵ�д�
����ѧ��Ӯ�����ϵ�д�