题目内容
一定质量溶质质量分数为19.6%的硫酸溶液与此同时13克锌恰好完全反应.试回答下列问题:(1)求硫酸溶液的质量.
(2)根据题条件,你还能求出______(写出一个问题,并解答)
【答案】分析:根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查.在本题中,已知锌的质量,可以求出硫酸的质量,再根据质量分数公式求出硫酸溶液的质量;根据题条件,还能求出氢气的质量,硫酸锌的质量或质量分数等.
解答:解:设硫酸的质量为x,生成氢气的质量为y
Zn+H2SO4=ZnSO4+H2↑
65 98 2
13g x y
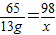 x=19.6g
x=19.6g  y=0.4g
y=0.4g
19.6g÷19.6%=100g 答:硫酸溶液的质量是100g,氢气的质量是0.4g.
故答案为:(1)100g,(2)氢气的质量是0.4g.
点评:本考点考查了根据化学方程式的计算,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,本考点主要出现在计算题中.
解答:解:设硫酸的质量为x,生成氢气的质量为y
Zn+H2SO4=ZnSO4+H2↑
65 98 2
13g x y
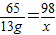 x=19.6g
x=19.6g  y=0.4g
y=0.4g19.6g÷19.6%=100g 答:硫酸溶液的质量是100g,氢气的质量是0.4g.
故答案为:(1)100g,(2)氢气的质量是0.4g.
点评:本考点考查了根据化学方程式的计算,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,本考点主要出现在计算题中.

练习册系列答案
相关题目
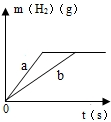 已知钠、钾都是活泼金属,都能与水反应生成氢气和对应的碱.将一定质量的钠、钾分别投入质量相等的足量的纯水中,产生氢气的质量随时间变化的曲线如图所示.下列说法错误的是( )
已知钠、钾都是活泼金属,都能与水反应生成氢气和对应的碱.将一定质量的钠、钾分别投入质量相等的足量的纯水中,产生氢气的质量随时间变化的曲线如图所示.下列说法错误的是( )| A、曲线a表示钠与水反应的图象,曲线b表示钾与水反应的图象 | B、参加反应的钠的质量大于钾的质量 | C、参加反应的水的质量相等 | D、反应后NaOH溶液的溶质质量分数小于KOH溶液的溶质质量分数 |
2009年9月,中国经济时报报道,在汶川地震灾区的建筑用砖放置一段时间后,就变成脆弱的粉粉砖.经调查,当地用来烧砖的页岩矿中含石灰石超标,取100g这种页岩矿盛于烧杯中,将200g一定质量分数的稀盐酸分成相等的四份逐渐加入,每次加入充分反应后,烧杯中所盛物质的质量如下表所示:
试计算:
(1)所用稀盐酸的溶质质量分数
(2)所取的页岩矿中钙元素的质量分数是多少?
| 次 数 | 第一次 | 第二次 | 第二次 | 第四次 |
| 烧杯内容物的质量 | 145.6g | 191.2g | 236.8g | 284.6g |
(1)所用稀盐酸的溶质质量分数
(2)所取的页岩矿中钙元素的质量分数是多少?