题目内容
【题目】无论在化学世界里,还是在日常生活中,酸是广泛存在而又非常重要的物质。下面对常见的酸——硫酸的部分性 质进行探究。
(1)浓硫酸的特性
①向一个烧杯中加入一定质量的浓硫酸,总质量为m1;敞口放置在空气中一段时间后,总质量为m2,那么,m1_____m2(选填“>、=、<")。
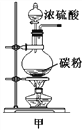
②如图所示,将水滴入装有浓硫酸的锥形瓶中(锥形瓶和木板用熔化的石蜡粘在一起),观察到液滴四溅。据此分析,下列关于浓硫酸的叙述正确的是____。
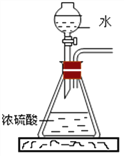
A.稀释浓硫酸时, 一定要将浓硫酸缓慢注入水中
B.稀释浓硫酸时,一定要 将水缓慢注入浓硫酸中
C.浓硫酸充分溶于水后,可以将锥形瓶从木板上轻轻提离
(2)与金属反应
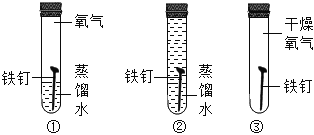
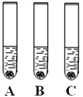
向装有镁、铁、铜的A、B、C三只试管中(如图),分别加入等质量等质量分数的稀硫酸,不能观察到明显现象的是______(填序号);请写出反应最剧烈的试管中发生反应的化学方程式___________。
(3)与非金属反应
将冷的浓硫酸加入到装有碳粉的圆底烧瓶中,无明显现象;加热该混合物,有大量气泡产生,现对导出的气体成分进行验证。
(查阅资料)
①碳与浓硫酸在加热时,除了生成水之外,还生成二氧化碳和碳的一种氧化物;
②二氧化硫和二氧化碳都能使澄清石灰水变浑浊,其中二氧化硫还能使紫红色的酸性高锰酸钾溶液褪色。
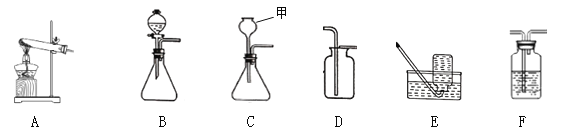
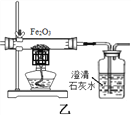
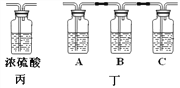
(实验验证)某化学兴趣小组在老师指导下设计了如下实验装置进行验证。
温馨提示:丁装置的A、B、C中均装有紫红色的酸性高锰酸钾溶液
![]()
①为了完成对导出气体的验证,请将上述装置进行正确的连接:甲→______→______丙→_______(填序号)。
②请完成下表中的相关内容:
实验现象 | 实验结论 |
乙中观察到的现象_______ | 证明碳与浓硫酸加热反应生成碳的氧化物是二氧化碳而不是一氧化碳 |
丁装置A中溶液褪色 丁装置C中溶液不褪色 | 证明气体中有___________ 装置C的作用______________ |
戊中白色固体变蓝 | 证明气体中有水蒸气 |
(获得结论)碳与浓硫酸加热反应的化学方程式__________。
(知识拓展)化学反应的进行与反应物的溶质质量分数、反应条件都有一定关系。酸不仅仅能与某些金属反应,还能与某些非金属单质在一定条件下反应。
【答案】 < A C C Mg+H2SO4=MgSO4+H2↑ 戊 丁 乙 乙中红色粉末不变色,澄清石灰水变浑浊 二氧化硫或SO2 证明SO2被除净 C+2H2SO4 △ CO2↑+2SO2↑+2H2O
【解析】(1)①浓硫酸具有吸水性,故将浓硫酸置于空气中质量增加,m12;
②稀释浓硫酸时,要将浓硫酸慢慢的注入水中,故A正确,B错误,浓硫酸溶于水是强放热过程,故锥形瓶底部的石蜡融化,故C正确。故选AC;
(2)在金属活动性顺序表中,铜在氢的后面,故C试管中无明显现象;镁比铁活泼,故装有镁的试管反应最剧烈,反应方程式为Mg+H2SO4=MgSO4+H2↑;
(3)①为了验证反应中有水生成,后面的装置中都有水带出,故要先检验水的生成,需要先经过戊装置,检验有水生成,然后经过丁装置检验并除尽二氧化硫,最后剩余的气体中可能有一氧化碳和二氧化碳,通入乙装置;②如不是一氧化碳,则乙中红色粉末不变色,澄清石灰水变浑浊;丁装置A中溶液褪色,说明溶液中一定有二氧化硫气体;丁装置C中溶液不褪色,说明二氧化硫被完全吸收;碳与浓硫酸在加热的条件下反应生成二氧化碳、二氧化硫和水,反应方程式为C+2H2SO4 △ CO2↑+2SO2↑+2H2O。

【题目】氢化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通过查阅资料得知:氢化钙![]() 遇水反应生成氢氧化钙和氢气。探究斯小组的同学把一定量的
遇水反应生成氢氧化钙和氢气。探究斯小组的同学把一定量的![]() 加入
加入![]() 溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
(提出问题)滤液中溶质的成分是什么?
猜想一:NaOH猜想二:NaOH、![]()
猜想三:NaOH、![]() 猜想四:NaOH、
猜想四:NaOH、![]() 、
、![]()
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因______。
(实验验证)
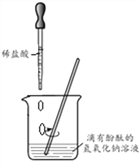
实验 | 现象 | 结论 |
| 无明显现象 | 猜想 ______ 不成立 |
| ______ | 猜想三成立 |
(反思与拓展)
![]() 写出氢化钙
写出氢化钙![]() 与水反应的化学方程式______。
与水反应的化学方程式______。
![]() 若向
若向![]() 的溶液中加入一定量的
的溶液中加入一定量的![]() ,充分反应,产生的气体有氢气和______。
,充分反应,产生的气体有氢气和______。
![]() 登山运动员携带
登山运动员携带![]() 作为能源提供剂与携带氢气相比,其优点是______
作为能源提供剂与携带氢气相比,其优点是______![]() 写一条即可
写一条即可![]() 。
。
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)工业上生产尿素[CO(NH2)2]的反应微观示意图如下:
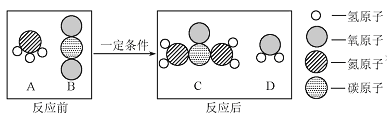
①从微观角度着,上图中四种物质都是由__________构成;
②从宏观的角度看,上图四种物质中属于氧化物的有__________(填字母序号);
③写出工业上生产尿素的化学方程式___________________________________________。
(2)下表是元素周期表中第2、3周期的元素,请回答有关问题。
2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
3 | Na 钠 22.99 | Mg 镁 24.31 | Al 铝 26.98 | Si 硅 28.09 | P 磷 30.97 | S 硫 32.06 | Cl 氯 35.45 | Ar 氩 39.95 |
①下列各组具有相似化学性质的元素是__________(填字母序号);
A.Na、Cl B.O、S C.F、Cl D.Cl、Ar
②写出一条第三周期元素原子的核外电子排布规律_____________________________;
③第7号元素与第l2号元素的原子形成化合物的化学式为_______________;
④某粒子的结构示意图为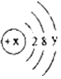 ,当x-y=8时,该粒子的符号为_____________;
,当x-y=8时,该粒子的符号为_____________;
⑤具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是__________(填字母序号)。
A.NO和O2 B.CO和N2 C.SO2和CO2 D.PO43-和SO42-