题目内容
【题目】铁、铜、银、锌是生活中常见的金属,请根据所学知识回答下列问题.
(1)铜能制成导线,是利用了铜的性.
(2)若要验证Cu、Ag、Fe的活动性强弱,可选择的试剂组是(填序号)
A.Fe、Cu、Ag、稀硫酸
B.Cu、Ag、FeSO4溶液
C.Fe、Ag、CuSO4溶液
(3)将等质量的锌粉和铁粉分别与溶质质量分数相同等质量的稀硫酸充分反应,产生H2的质量与时间的关系如图所示.请回答下列问题: ①表示锌粉与稀硫酸反应的曲线是(填“a”或“b”).
②对于曲线a表示的反应,(填化学式)有剩余.
③若有一种金属有剩余,则剩余的金属一定是填化学式.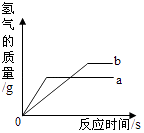
【答案】
(1)导电
(2)C
(3)a;H2SO4;Fe
【解析】解:(1)铜能制成导线,是利用了铜的导电性.(2)A、把铁插入稀硫酸中,有气泡产生,说铁在氢的前面,把铜和银插入硫酸溶液中,没有现象,说明铜和银在氢的后面,不能说明铜和银的活动性,错误;
B、把铜和银插入硫酸亚铁溶液中,没有现象,说明铜和银在铁的后面,但是不能说明铜和银的活动性,错误;
C、把铁插入硫酸铜溶液中,铁的表面有红色物质析出,说明铁的活动性大于铜;把银放入硫酸铜溶液中,银的表面无变化,说明银的活动性小于铜,能验证Cu、Ag、Fe的活动性强弱,故正确.(3)①根据图示,在停止反应前的时间段,相同时间内曲线a代表的金属产生氢气的速度大于曲线b代表的金属,说明金属a的活动性大于金属b,锌的活动性比铁强,所以金属a为锌;②从图示看出,锌和铁与酸反应后生成的氢气质量不同,如果硫酸完全反应的话,生成的氢气质量应该相同,现在锌生成的氢气少,故推知硫酸没有完全和锌反应,有剩余;
③56gFe消耗98g硫酸,65gZn消耗98g硫酸,假设硫酸的质量均为98g,金属的质量均为65g,则明显Fe只需要消耗56g,Zn需要消耗全部,即等质量的硫酸消耗Fe的质量少,则剩余的是铁.
所以答案是:(1)导电;(2)C;(3)①a;②H2SO4;③Fe.
【考点精析】认真审题,首先需要了解金属的物理性质及用途(金属的物理性质: (1)常温下一般为固态(汞为液态),有金属光泽.(2)大多数呈银白色(铜为紫红色,金为黄色)(3)有良好的导热性、导电性、延展性),还要掌握金属材料的选择依据(黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属)的相关知识才是答题的关键.

 名校课堂系列答案
名校课堂系列答案【题目】实验室常用的气体发生装置如下:
(1)装置A的名称 , 用该装置制取二氧化碳气体的化学方程式是 .
(2)搭建B装置时,酒精灯应在固定试管之(填“前”或“后”)放置. 
(3)用粉末状二氧化锰和3%的过氧化氢溶液混合制取氧气的化学方程式 , 用C装置进行该反应时,为较好地控制氧气的产生速率,应采取的操作是 . 
(4)在研究实验室制取二氧化碳的过程中,进行了如下实验:
实验编号 | 甲 | 乙 | 丙 | 丁 |
大理石 | m g,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
盐酸(过量) | w g,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
①研究盐酸浓度大小对反应速率的影响,可选择实验甲与实验进行对比实验(选填实验编号).
②上述实验说明影响反应速率的因素有浓度、 .
③实验丁最后所得溶液的质量小于实验甲最后所得溶液的质量,其原因是 .