题目内容
 (2006?佛山)为测定H2SO4与NaOH发生中和反应时敞出的热量,在右图的小烧杯中装入一定量的NaOH,测其温度;另取一定量的硫酸,测其温度,并缓慢地倾入小烧杯中,边加边用环形玻璃搅拌棒搅拌.记录溶液温度的变化.甲、乙、丙三位同学准备选择以下试剂进行实验:
(2006?佛山)为测定H2SO4与NaOH发生中和反应时敞出的热量,在右图的小烧杯中装入一定量的NaOH,测其温度;另取一定量的硫酸,测其温度,并缓慢地倾入小烧杯中,边加边用环形玻璃搅拌棒搅拌.记录溶液温度的变化.甲、乙、丙三位同学准备选择以下试剂进行实验:| 同学\使用的试剂 | 使用的NaOH | 使用的H2SO4 |
| 甲 | NaOH固体 | 稀H2SO4 |
| 乙 | NaOH溶液 | 浓H2SO4 |
| 丙 | NaOH溶液 | 稀H2SO4 |
(1)
甲
甲
同学错误的原因是NaOH固体溶于水时会放出热量,对测量产生误差
NaOH固体溶于水时会放出热量,对测量产生误差
;(2)
乙
乙
同学错误的原因是浓硫酸溶于水时会产生大量的热,对测量产生误差
浓硫酸溶于水时会产生大量的热,对测量产生误差
.分析:根据物质的性质进行分析,氢氧化钠固体和浓硫酸溶于水会放热.
解答:解:(1)甲同学使用的氢氧化钠固体溶于水会放出热量,所以本题答案为:甲,NaOH固体溶于水时会放出热量,对测量产生误差;
(2)乙同学使用的浓硫酸溶于水会放出热量,所以本题答案为:乙,浓硫酸溶于水时会产生大量的热,对测量产生误差.
(2)乙同学使用的浓硫酸溶于水会放出热量,所以本题答案为:乙,浓硫酸溶于水时会产生大量的热,对测量产生误差.
点评:本题考查了常见物质的性质,完成此题,可以依据已有的知识进行,要求同学们在平时的学习中加强基础知识的储备,以便灵活应用.

练习册系列答案
相关题目
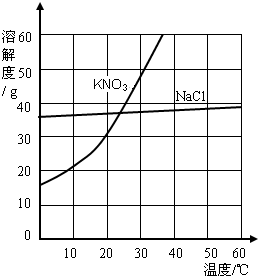 (2006?佛山)右图是KNO3和NaCl在水中的溶解度曲线.
(2006?佛山)右图是KNO3和NaCl在水中的溶解度曲线.
 (2006?佛山)2006年4-5月间,我省多名患者因注射某制药公司生产的假药“亮菌甲素注射液”而死亡.造成该事件的原因是该制药公司在购买药用辅料丙二醇时,购入了二甘醇假冒丙二醇以至酿成悲剧.根据右图标签作答.
(2006?佛山)2006年4-5月间,我省多名患者因注射某制药公司生产的假药“亮菌甲素注射液”而死亡.造成该事件的原因是该制药公司在购买药用辅料丙二醇时,购入了二甘醇假冒丙二醇以至酿成悲剧.根据右图标签作答.