题目内容
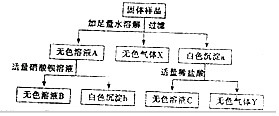
【题目】工业生产中,用焦炭与水蒸气在高温条件下反应制取水煤气,水煤气中一定含有水蒸气,可能含有H2、CO和CO2中的一种或几种,为探究其成分,实验过程如图所示,回答问题: 
(1)A装置中,足量澄清石灰水的作用是;
(2)向D处烧杯中滴入澄清石灰水并振荡,目的是检验水煤气中成分是否存在;
(3)如果水煤气中含有H2、CO和CO2验证含有H2 , 依据的实验现象是;
(4)如果将A装置和B装置连接顺序颠倒,会影响水煤气中成分的验证.
【答案】
(1)证明二氧化碳的存在
(2)一氧化碳
(3)看到烧杯内壁上有水珠出现
(4)氢气
【解析】解:(1)二氧化碳能使澄清石灰水变浑浊可以证明二氧化碳的存在;故填:证明二氧化碳的存在;(2)一氧化碳燃烧生成二氧化碳,二氧化碳能使澄清石灰水变浑浊能证明一氧化碳存在;故填:一氧化碳;(3)氢气燃烧生成水,看到烧杯内壁上有水珠出现能证明H2存在;故填:看到烧杯内壁上有水珠出现;(4)A中的澄清石灰水验证二氧化碳的存在,B中盛放的是浓硫酸为了消除水蒸气的影响,如果A、B装置的顺序调换,则不能除去水蒸气,影响对氢气的检验,所以不能调换;故填:氢气.

练习册系列答案
相关题目