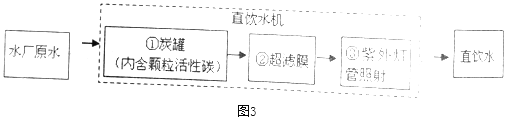
题目内容
【题目】在宏观、微观和符号之间建立联系是化学学科的特点.
(1)用化学用语填空
1个氮分子________;2个氢氧根离子_______;氯化镁中镁元素的化合价__________;
(2)氯化钠、铁、过氧化氢三种物质中,由离子构成是______.
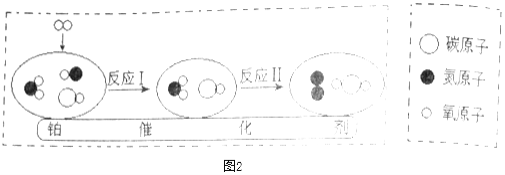
(3)A、B、C、D表示四种物质中,在高温条件下,A和B反应生成C和D,微观示意图如下图所示
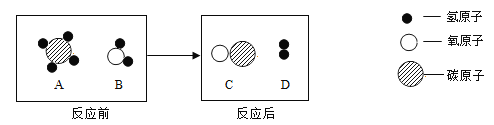
①每个A分子是由_____个原子构成的。
②反应后,生成C和D两种粒子的个数比应为______。
③下列结论中,正确的是_____________(填序号).
a.B和C属于氧化物 b.反应前后各元素化合价均发生改变
C.反应前后分子的个数没有改变 d.A物质中氢元素的质量分数为25%
【答案】N2 2OH- ![]() 氯化钠(或NaCl) 5 1∶3 ad
氯化钠(或NaCl) 5 1∶3 ad
【解析】
(1)氮气化学式为N2,1个氮分子故填N2;氢氧根离子带一个单位的负电荷,在离子符号前加上数字就表示离子的个数,故填2OH-;氯化镁中镁元素显+2价,故填![]() ;
;
(2)氯化钠是由钠离子和氯离子构成的离子型化合物,铁是由铁原子直接构成的,过氧化氢是由分子构成的物质,故填氯化钠(或NaCl);
(3)
①有图示可知每个A分子中含有5个原子,故填5;
②由题图可知反应物是甲烷和水,生成物是一氧化碳和氢气,方程式为CH4+ H2O ![]() CO+3 H2,可知生成C和D两种粒子的个数比为1∶3,故填1∶3;
CO+3 H2,可知生成C和D两种粒子的个数比为1∶3,故填1∶3;
③
a、B是水,C是一氧化碳,都属于氧化物,故选项正确;
b、根据各物质的化学式可知,反应前后氧元素化合价没有发生改变,故选项不正确;
c、根据化学方程式可知,反应前是2个分子,反应后是4个分子,分子个数改变,故选项不正确;
d、A物质中氢元素的质量分数=![]() ×100%= 25%,故选项正确;故填ad。
×100%= 25%,故选项正确;故填ad。

【题目】酸和碱能发生中和反应,它在日常生活和工农业生产中有着广泛的应用。下图表示硫酸和氢氧化钠溶液发生反应时烧杯中溶液的pH随加入液体体积的变化曲线及相关的实验操作。请从中获取信息,回答下列问题:
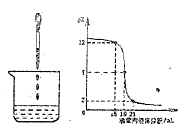
(1)烧杯中盛放的是______溶液。
(2)小明向氢氧化钠溶液中加入稀硫酸,该中和反应的实质是______。然后,对反应过程中废液的溶质进行了如下探究:
(提出问题)氢氧化钠溶液和稀硫酸混合后,溶质是什么?
(查阅资料)硫酸钠溶液呈中性
(猜想假设)猜想I硫酸钠和氢氧化钠;猜想Ⅱ硫酸钠和硫酸;猜想Ⅲ______。
(设计实验)
实验操作 | 实验现象 | 实验结论 |
①取少量废液于试管中,滴入几滴酚酞试液 | 溶液无明显变化 | 猜想______不成立 |
②另取少量废液于试管中,滴入几滴氯化钡溶液 | ______ | 猜想Ⅱ成立 |
(反思与评价)小芳认为实验操作②得出的结论不成立,理由是______。可以改为向废液中加入少量______,溶液变为红色,证明猜想Ⅱ成立