��Ŀ����
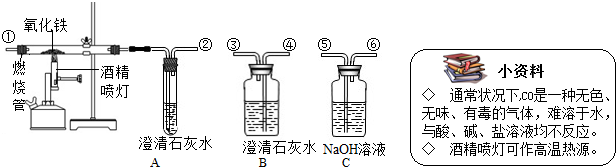
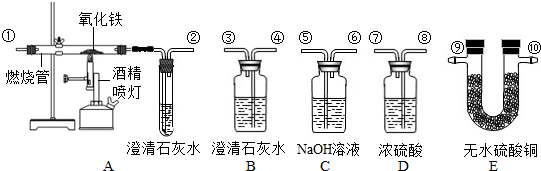
��ȷ��������ͼ��ʾ��װ�ý���ʵ�飬������֤mgij�������ijɷ���CO2��H2O��CO�������Բ��ÿ�������������ÿ��װ������һ�Σ���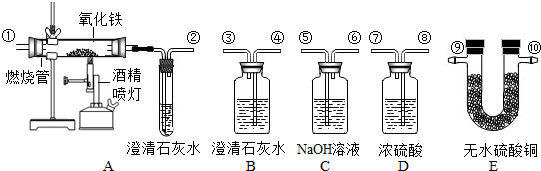
| С���� 1��ͨ�������CO���ᡢ�����Һ������Ӧ�� 2����ˮ����ͭ�ǰ�ɫ���壬����ˮ���������ɫ���壮��ش��������⣺ ��1�����ӵ��ܿڣ���-�⣩˳�������� ��2��֤��ԭ���������CO���ڵ�ʵ�������� ��3�������Բ�ö�����̼������Ӧ���еIJ����� ��������1�����ݼ���ˮ�������ȣ���ˮ�����ں��������Ƴ����������̼���������Ƴ�������̼��ԭ����з����� ��2������һ����̼�Ὣ��������ԭ��������̼����������������̼��ƽ��з��������ݷ�Ӧ��������Լ���Ӧ����������д����ʽ�� ��3������B��C��Ӧ������ն�����̼���������з����� ����⣺��1��������װ�ü��������̼���ó���ʯ��ˮ���飬������̼��ʯ��ˮ��Ӧ����ֻ��ǣ���ȥ������̼ѡ���������ƣ�����������ˮ�е��ܽ�Ƚϴ�����Ч���Ϻã�Ҫ�ȼ���ˮ�Ĵ��ڣ���ȥˮ��Ҫ��������Ǵ���Ҫ�����֪��ÿ�����������������Ӧ�ý�Ũ�������������ڶ�����̼�ļ��������֮ǰ������Ӧ��ǰ�ã���������ͭ��������������ӿ���֪��ˮ������������������������Һ������������Һ���������ӿ���ȷ��������̼��������һ����̼����ͨ������װ�ý��м��㣮�ʴ�Ϊ������ߢܢۢݢޢ٢ڣ� ��2��һ����̼���л�ԭ�ԣ����Խ���������ԭ�������Ͷ�����̼��������̼��ʹ����ʯ��ˮ����ǣ��������Ǻ�ɫ�����Ǻ�ɫ�ģ��ʴ�Ϊ��A�к�ɫ��ĩ��ڣ�����ʯ��ˮ����ǣ� һ����̼���������ڸ��µ��������������Ͷ�����̼��������̼���������Ʒ�Ӧ���ɰ�ɫ��̼��Ƴ�����ˮ���ʴ�Ϊ��3CO+Fe2O3
��3������ʯ��ˮ��Ϊ�˼��������̼�Ĵ��ڣ���������һ���ֶ�����̼�����������������ն�����̼���������ӵ��������Ƕ�����̼���������ʴ�Ϊ����ʵ��ǰ����װ��B��C����������ʵ����ٳ���B��C��������������ʵ��ǰ��B��C�������ı仯ֵ�����ֵ���� ������������Ҫ�����˳�������ļ���ͳ��ӵķ��������������̼�ó���ʯ��ˮ����ȥ������̼���������ƣ� 
��ϰ��ϵ�д�
�����Ŀ
|