题目内容
【题目】根据如图所示的甲、乙两物质溶解度曲线,判断下列说法中正确的是( ) 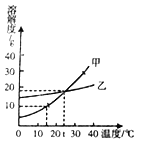
A.t℃时,甲、乙溶液的浓度一定相等
B.10℃时,甲的溶解度一定大于乙
C.15℃时,11g甲的饱和溶液中溶质质量为1g
D.t℃时,用20g的甲配得的溶液一定是饱和溶液
【答案】C
【解析】解:A、t℃时,甲、乙物质的溶解度相等,饱和溶液的浓度一定相等,故A错误; B、通过分析溶解度曲线可知,10℃时,甲的溶解度小于乙,故B错误;
C、15℃时,甲物质的溶解度是10g,所以11g甲的饱和溶液中溶质质量为1g,故C正确;
D、t℃时,溶剂的质量不能确定,所以用20g的甲配得的溶液不一定是饱和溶液,故D错误.
故选:C.
【考点精析】利用固体溶解度曲线及其作用对题目进行判断即可得到答案,需要熟知1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).

 口算题天天练系列答案
口算题天天练系列答案【题目】过氧化钠(Na2O2)可用作呼吸面具中的供氧剂,实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究.
【查阅资料】过氧化钠能与空气中的水和二氧化碳反应生成氧气:2Na2O2+2H2O═4NaOH+O2↑,2Na2O2+2CO2=2NaCO3+O2 .
【提出问题】过氧化钠是否变质?
【猜想与假设】
假设1:过氧化钠未变质;假设2:过氧化钠部分变质;假设3:过氧化钠全部变质.
(1)【实验探究】
序号 | 实验步骤 | 实验现象 | 实验结论 |
① | 取部分固体于试管中,加入适量的水,在试管口插入带火星的木条 | 固体完全溶解,木条复燃 | 假设不成立 |
② | 取少量①中溶液于试管中,滴加足量的 , 振荡 | 有气泡生成 | 假设2成立 |
(2)【提出新问题】部分变质的过氧化钠样品中是否含有氢氧化钠呢?
【实验探究】
实验③:取少量①中溶液于试管中,加入足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】
由实验③可以确定①中溶液含有的溶质是(填化学式).
(3)小明认为,由上述实验无法确定原固体药品中是否含有氢氧化钠,理由是 .
(4)【定量分析】
称取6.04g过氧化钠药品于锥形瓶中,加入适量蒸馏水使固体完全溶解,共收集到0.64g气体;再向上述锥形瓶中加入足量的澄清石灰水,充分反应,经过滤、干燥等操作,称量固体质量为2.00g.
写出加入澄清石灰水发生反应的化学方程式:;
(5)6.04g上述样品中含有NaOH的质量为 g.
(6)【反思提高】
过氧化钠长时间露置在空气中会全部变质,最终转化为(填化学式).