题目内容
【题目】实验室中加热氯酸钾和二氧化锰的混合物可制得氧气,在制备过程中,MnO2在混合物中的质量分数随加热时间的变化图像如图所示。
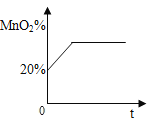
(1)当MnO2的质量分数达到多少时不再产生氧气_______?
(2)当反应完毕后剩余固体的质量为10.5g,则产生氧气多少克_______?
【答案】29.1% 4.8
【解析】
(1)假设反应前混合物的质量为100g,则二氧化锰的质量为20g,氯酸钾的质量为80g。
设80g氯酸钾完全反应生成氯化钾的质量为x
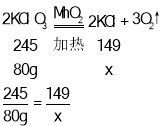
解得:x=48.7g
所以反应后二氧化锰的质量分数为:![]() ×100%=29.1%
×100%=29.1%
(2)若剩余固体的质量为10.5g,则可以知道生成氯化钾的质量为:10.5g×(1-29.1%)=7.45g
设可生成氧气的质量为y,则:
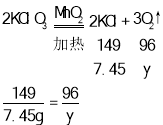
解得:y=4.8g
答:(1)当MnO2的质量分数达到29.1%时不再产生氧气;
(2)当反应完毕后剩余固体的质量为10.5g,则产生氧气4.8克。

 阅读快车系列答案
阅读快车系列答案【题目】铬(Cr)是一种重要的金属材料,它具有良好的金属光泽和抗腐蚀性,常用来镀在其他金属的表面上,铜、铬、锰、镍组成合金可以制成各种性能的不锈钢。某校化学研究小组对Cr(铬)、Al、Cu的金属的活动性顺序进行探究,过程如下:
(作出假设)对三种金属的活动性顺序提出三种可能的假设:
①Cr>Al>Cu;②Al>Cr>Cu;③__________。
(设计实验)同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象, 记录如下:
金属 | Cr | Al | Cu |
与盐酸反应现 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | ___________ |
(控制实验条件)三种金属加入盐酸前都先用纱布将其表面擦光亮,其目的是(_____)
A除去氧化膜,利于直接反应 B使表面光亮,易观察现象 C使金属温度相同,易反应
(得出结论)原假设中正确的是________(选填假设中①、②或③)。写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式:____________________。
(结论应用)(1)根据探究结果,请你预测铬与硫酸铜溶液____________(选填“能”或“不能”)发生反应理由是____________。
(2)铝的化学性质比较活泼,在空气中比铁更易被氧化,但铝制品比铁制品更耐用,是因为铝制品表面有一层致密的氧化铝保护膜,阻止铝进一步被氧化。食醋不宜用铝制品盛放,其原因是_________________。