题目内容
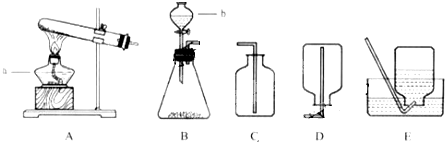
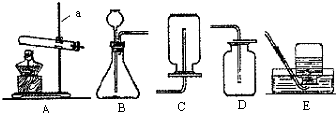
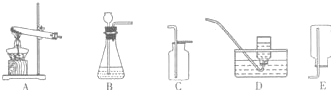
化学实验和科学探究都离不开实验装置.根据下列装置,回答问题:

(1)用A装置制取氧气的化学反应方程式是
(2)科学探究
查阅资料:小玲同学查阅资料发现:过氧化钙(CaO2)能分别与水、二氧化碳反应.
过氧化钙与水反应方程式为:2CaO2+2H2O=2Ca(OH)2+O2↑
猜想:过氧化钙在空气中久置生成的物质可能是碳酸钙或氢氧化钙或二者的混合物.
实验探究:
实验一:选用装置A进行过氧化钙与水反应的实验,收集气体;取反应后的溶液置于试管中,充分振荡后再滴入
实验二:为探究猜想是否正确,小玲设计了如下实验,请你帮助她完成表格中的空白内容:
实验步骤c中发生反应的化学方程式是
(3)在上述实验一中,若取过氧化钙(CaO2)7.2g加入足量水94.4g,充分反应,求得到溶液的溶质质量分数.

(1)用A装置制取氧气的化学反应方程式是
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.实验室使用稀盐酸和金属锌制取的氢气往往含有少量
| ||
HCl
HCl
和水蒸气杂质,欲收集纯净的氢气,所选装置的顺序为ABCE
ABCE
;(2)科学探究
查阅资料:小玲同学查阅资料发现:过氧化钙(CaO2)能分别与水、二氧化碳反应.
过氧化钙与水反应方程式为:2CaO2+2H2O=2Ca(OH)2+O2↑
猜想:过氧化钙在空气中久置生成的物质可能是碳酸钙或氢氧化钙或二者的混合物.
实验探究:
实验一:选用装置A进行过氧化钙与水反应的实验,收集气体;取反应后的溶液置于试管中,充分振荡后再滴入
酚酞
酚酞
(填写一种试剂的名称)试液,发现溶液变成红色.实验二:为探究猜想是否正确,小玲设计了如下实验,请你帮助她完成表格中的空白内容:
| 实验步骤 | 实验现象 | 结论 |
| a.取在空气中久置的少量固体于试管中,加足量水 | 未见固体明显溶解 | |
| b.向试管中滴加几滴紫色石蕊试液 | 未见明显的颜色变化 | 不存在氢氧化钙 |
| c. | 有气泡产生 | 固体成分是碳酸钙 |
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.(3)在上述实验一中,若取过氧化钙(CaO2)7.2g加入足量水94.4g,充分反应,求得到溶液的溶质质量分数.
分析:制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集,如果收集干燥的氢气,只能用向下排空气法收集;如果实验室使用稀盐酸和金属锌制取的氢气往往含有少量氯化氢气体和少量的水蒸气,要先除杂质再干燥,因此所选装置的顺序为ABCE.实验一,选用装置A进行过氧化钙与水反应的实验,收集气体;取反应后的溶液置于试管中,充分振荡后再滴入酚酞,试液,发现溶液变成红色;实验二,c.取少量固体,滴加稀盐酸,有气泡产生,固体成分是碳酸钙;发生反应的化学方程式是碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳;
解答:解:(1)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集,如果收集干燥的氢气,只能用向下排空气法收集;如果实验室使用稀盐酸和金属锌制取的氢气往往含有少量氯化氢气体和少量的水蒸气,要先除杂质再干燥,因此所选装置的顺序为ABCE;故答案为:2H2O2
2H2O+O2↑;HCl;ABCE;
(2)实验一,选用装置A进行过氧化钙与水反应的实验,收集气体;取反应后的溶液置于试管中,充分振荡后再滴入酚酞,试液,发现溶液变成红色;实验二,c.取少量固体,滴加稀盐酸,有气泡产生,固体成分是碳酸钙;发生反应的化学方程式是碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳;故答案为:酚酞;c.取少量固体,滴加稀盐酸;CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)解:设生成的氢氧化钙的质量为x,生成氧气质量为y
2CaO2+2H2O=2Ca(OH)2+O2↑
144 148 32
7.2g x y
=
x=7.4g
=
y=1.6g
所得溶液溶质质量分数为:
×100%=7.4%
答:所得溶液溶质质量分数为7.4%
故答案为:7.4%
| ||
(2)实验一,选用装置A进行过氧化钙与水反应的实验,收集气体;取反应后的溶液置于试管中,充分振荡后再滴入酚酞,试液,发现溶液变成红色;实验二,c.取少量固体,滴加稀盐酸,有气泡产生,固体成分是碳酸钙;发生反应的化学方程式是碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳;故答案为:酚酞;c.取少量固体,滴加稀盐酸;CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)解:设生成的氢氧化钙的质量为x,生成氧气质量为y
2CaO2+2H2O=2Ca(OH)2+O2↑
144 148 32
7.2g x y
| 144 |
| 148 |
| 7.2g |
| x |
| 144 |
| 32 |
| 7.2g |
| y |
所得溶液溶质质量分数为:
| 7.4g |
| 7.2g+94.4g-1.6g |
答:所得溶液溶质质量分数为7.4%
故答案为:7.4%
点评:本考点主要考查了气体的制取装置和收集装置的选择、气体的除杂和干燥,同时也考查了化学方程式的书写和根据化学方程式的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关,有关的计算要准确.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目