题目内容
【题目】如图所示,某实验小组进行以下实验: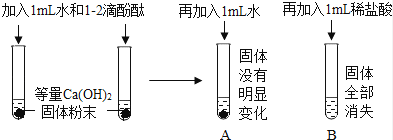
(1)上述实验进行对比的目的是 .
(2)实验后,将A、B两试管中的溶液倒入同一个洁净的烧杯中,溶液无色.再向其中加入一定量的碳酸钠溶液(提示:CaCl2+Na2CO3═CaCO3↓+2NaCl),所得混合物中溶液的溶质成分有四种情况,请补充完整(酚酞省略不写):①NaCl;② ;③ ;④ .若该混合物中溶液无色,选用一种试剂即可确定溶质成分是哪种情况,写出所加试剂,预期现象和结论 .
【答案】
(1)说明盐酸和氢氧化钙发生了反应而非溶于水
(2)NaCl、CaCl2;NaCl、Na2CO3;NaCl、CaCl2、HCl;取少量混合液,向其中加入碳酸钠溶液,无明显现象为①,有白色沉淀为②,有气泡产生为④
【解析】②解:(1)据图示加入1mL水固体没有明显变化,而加入1mL稀盐酸固体却全部消失,说明盐酸和氢氧化钙发生了反应而非溶于水;
(2)若氢氧化钙与盐酸恰好完全反应,生成氯化钙和水,所加碳酸钠也与氯化钙恰好完全反应,此时溶液中的溶质只有NaCl;
若氢氧化钙与盐酸恰好完全反应,生成氯化钙和水,所加碳酸钠较少,氯化钙有剩余,此时溶液中的溶质有NaCl、CaCl2;
若氢氧化钙与盐酸恰好完全反应,生成氯化钙和水,所加碳酸钠过量,此时溶液中的溶质有NaCl、Na2CO3;
若氢氧化钙与盐酸反应,盐酸有剩余,所加碳酸钠也与盐酸反应,且反应完毕后盐酸继续有剩余,此时溶液中的溶质有NaCl、CaCl2、HCl;
若氢氧化钙与盐酸反应,盐酸有剩余,所加碳酸钠也与盐酸恰好完全反应,此时溶液中的溶质只有NaCl;
溶液无色,说明溶液不显碱性,故溶液中不含有Na2CO3;可选用碳酸钠溶液进行测试,取少量的待测溶液放于试管中,滴加少量的碳酸钠溶液,无任何现象时为①;若出现白色沉淀为②;若有气泡产生为④.
所以答案是:(1)盐酸和氢氧化钙发生了反应而非溶于水;(2)②NaCl、CaCl2;③NaCl、Na2CO3④NaCl、CaCl2、HCl;取少量混合液,向其中加入碳酸钠溶液,无明显现象为①,有白色沉淀为②,有气泡产生为④.
【考点精析】掌握中和反应及其应用是解答本题的根本,需要知道中和反应:酸与碱作用生成盐和水的反应.

 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案


