题目内容
某课外小组的同学用下列装置探究二氧化碳的实验室制法.

(1)检验B装置气密性的方法是 .
(2)用大理石与稀盐酸反应制取CO2,应该选用的发生和收集装置是 ,发生反应的化学方程式为 .
(3)查阅资料发现:加热固体碳酸氢钠(NaHCO3)也能制得二氧化碳(反应原理为:2NaHCO3
Na2CO3+H2O+CO2↑),此时应选用的发生装置是 .检验该反应是否有二氧化碳生成的方法是 .(用化学方程式表示)

(1)检验B装置气密性的方法是
(2)用大理石与稀盐酸反应制取CO2,应该选用的发生和收集装置是
(3)查阅资料发现:加热固体碳酸氢钠(NaHCO3)也能制得二氧化碳(反应原理为:2NaHCO3
| ||
考点:二氧化碳的实验室制法,检查装置的气密性,二氧化碳的检验和验满,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)从先用止水夹把导气管夹住,然后向长颈漏斗中不断加入水,如果水不能充满整个锥形瓶,说明装置的气密性好,否则,装置漏气去分析解答;
(2)从大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳反应不需要加热,二氧化碳气体的密度比空气大、能溶于水去分析解答;
(3)从加热固体碳酸氢钠(NaHCO3)也能制得二氧化碳,反应需要加热,通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水去分析解答.
(2)从大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳反应不需要加热,二氧化碳气体的密度比空气大、能溶于水去分析解答;
(3)从加热固体碳酸氢钠(NaHCO3)也能制得二氧化碳,反应需要加热,通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水去分析解答.
解答:解:(1)先用止水夹把导气管夹住,然后向长颈漏斗中不断加入水,如果水不能充满整个锥形瓶,说明装置的气密性好,否则,装置漏气;故答案为:先用止水夹把导气管夹住,然后向长颈漏斗中不断加入水,如果水不能充满整个锥形瓶,说明装置的气密性好;
(2)大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳.其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;由于实验室制二氧化碳的反应条件是不需要加热,故发生装置为B,二氧化碳气体的密度比空气大、能溶于水,故只能用向上排空气法而不能用排水法,去分析解答;故收集装置为C;故答案为:BC CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)加热固体碳酸氢钠(NaHCO3)也能制得二氧化碳,由于反应需要加热,所以发生装置应选A;通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水,其化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;故答案为:A CO2+Ca(OH)2=CaCO3↓+H2O.
(2)大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳.其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;由于实验室制二氧化碳的反应条件是不需要加热,故发生装置为B,二氧化碳气体的密度比空气大、能溶于水,故只能用向上排空气法而不能用排水法,去分析解答;故收集装置为C;故答案为:BC CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)加热固体碳酸氢钠(NaHCO3)也能制得二氧化碳,由于反应需要加热,所以发生装置应选A;通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水,其化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;故答案为:A CO2+Ca(OH)2=CaCO3↓+H2O.
点评:实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度.

练习册系列答案
相关题目
下列实验基本操作中正确的是( )
A、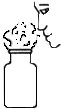 闻气体气味 |
B、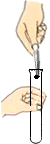 取用块状固体 |
C、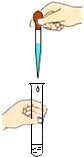 滴加液体 |
D、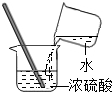 稀释浓硫酸 |
从防止空气污染考虑,下列实验应在通风橱中进行的是( )
A、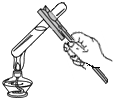 碘的受热和冷却 |
B、 白磷的燃烧 白磷的燃烧 |
C、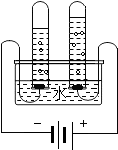 电解水 |
D、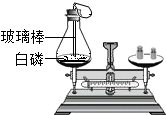 白磷燃烧前后质量测定 |
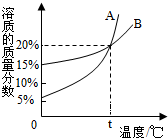 如图是A、B两种物质的饱和溶液的溶质的质量分数随温度变化的曲线,现将20gA和40gB分别置于100g水中,加热使其完全溶解,然后再冷却到t℃,下列有关叙述中正确的是( )
如图是A、B两种物质的饱和溶液的溶质的质量分数随温度变化的曲线,现将20gA和40gB分别置于100g水中,加热使其完全溶解,然后再冷却到t℃,下列有关叙述中正确的是( )| A、t℃时,A溶液的溶质的质量分数小于B |
| B、t℃时,A溶液的溶质的质量分数等于B |
| C、t℃时,两溶液中均无固体物质析出 |
| D、t℃时,二者的溶解度相等 |
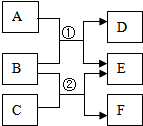 A~F表示初中化学常见的物质,A与B、B与C能发生反应且都只生成两种产物,它们之间的转化关系如图所示.
A~F表示初中化学常见的物质,A与B、B与C能发生反应且都只生成两种产物,它们之间的转化关系如图所示.