题目内容
某同学要配制80g质量分数为16%氯化钠溶液,步骤如下,请回答下列问题:
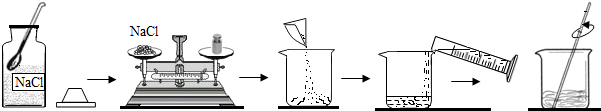
(1)用托盘天平称取氯化钠 g,准确量取所需水的仪器是 .
(2)实验中用到玻璃棒的目的是 .
(3)某同学实际配制的氯化钠溶液中溶质的质量分数低于16%,可能的原因是 .
A.量取水时仰视读数
B.称量氯化钠固体时把砝码放在左盘
C.配制溶液的烧杯用少量蒸馏水润洗
D.把已配好的溶液转移到细口瓶贮存时,有少量溶液溅出
(4)某同学要将50g质量分数为16%氯化钠溶液稀释为2%的氯化钠溶液,需要加水的质量为 g.

(1)用托盘天平称取氯化钠
(2)实验中用到玻璃棒的目的是
(3)某同学实际配制的氯化钠溶液中溶质的质量分数低于16%,可能的原因是
A.量取水时仰视读数
B.称量氯化钠固体时把砝码放在左盘
C.配制溶液的烧杯用少量蒸馏水润洗
D.把已配好的溶液转移到细口瓶贮存时,有少量溶液溅出
(4)某同学要将50g质量分数为16%氯化钠溶液稀释为2%的氯化钠溶液,需要加水的质量为
分析:(1)根据溶液中溶质质量=溶液质量×溶液的质量分数结合量取水用量筒分析;
(2)根据实验中玻璃棒的作用分析,搅拌,加速固体溶解;
(3)所配制的氯化钠溶液溶质质量分数小于16%,是由于所取氯化钠质量偏小或所取水的体积偏大的原因所致的结果,据此逐一分析即可;
(4)根据溶液中溶质质量=溶液质量×溶液的质量分数,利用加水稀释前后溶液中溶质质量不变分析.
(2)根据实验中玻璃棒的作用分析,搅拌,加速固体溶解;
(3)所配制的氯化钠溶液溶质质量分数小于16%,是由于所取氯化钠质量偏小或所取水的体积偏大的原因所致的结果,据此逐一分析即可;
(4)根据溶液中溶质质量=溶液质量×溶液的质量分数,利用加水稀释前后溶液中溶质质量不变分析.
解答:解:(1)氯化钠溶液中氯化钠的质量为80g×16%=12.8g;水用量筒量取;
故答案为:12.8;量筒;
(2)玻璃棒在该实验中所起的作用是搅拌,加速固体溶解;
故答案为:搅拌,加速固体溶解;
(3)A、用量筒量取水时仰视读数,量取的水体积偏大,质量就偏大,溶质质量不变,因此溶质质量分数偏小,故可能;
B、称量氯化钠固体时把砝码放在左盘,因需要用到游码,会导致称量的氯化钠偏小,溶剂质量不变,所以溶质质量分数偏小,故可能;
C、配制溶液的烧杯用少量蒸馏水润洗,会导致溶剂质量增大,因为溶质质量不变,所以溶质质量分数偏小,故可能;
D、把已配好的溶液转移到细口瓶贮存时,有少量溶液溅出,因溶液具有均一性,所以溶质质量分数不变,故不可能;
故选ABC;
(4)设需加水质量为x,根据稀释前后溶质的质量不变,则
50g×16%=(50g+x)×2%
解得x=350g
故答案为:350.
故答案为:12.8;量筒;
(2)玻璃棒在该实验中所起的作用是搅拌,加速固体溶解;
故答案为:搅拌,加速固体溶解;
(3)A、用量筒量取水时仰视读数,量取的水体积偏大,质量就偏大,溶质质量不变,因此溶质质量分数偏小,故可能;
B、称量氯化钠固体时把砝码放在左盘,因需要用到游码,会导致称量的氯化钠偏小,溶剂质量不变,所以溶质质量分数偏小,故可能;
C、配制溶液的烧杯用少量蒸馏水润洗,会导致溶剂质量增大,因为溶质质量不变,所以溶质质量分数偏小,故可能;
D、把已配好的溶液转移到细口瓶贮存时,有少量溶液溅出,因溶液具有均一性,所以溶质质量分数不变,故不可能;
故选ABC;
(4)设需加水质量为x,根据稀释前后溶质的质量不变,则
50g×16%=(50g+x)×2%
解得x=350g
故答案为:350.
点评:配制溶液时,所得溶液质量分数偏小的主要原因是固体溶质质量偏小或溶剂水体积偏大,所得溶液质量分数偏大的原因固体溶质质量偏大或溶剂水的体积偏小.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
