��Ŀ����
����Ŀ����8�֣����������ڹ���������������Ҫ�����ã�ͼ1Ϊ�ߩ�15�ɻ����������������
��1�����Ͻ���������ɻ�����ǣ����Ͻ���ʵ���Ҫ�ŵ��� ��
��2����װǰ�������������⼣�߰ߣ���������ʴ��Ҫ����������е� ��ͬ���õĽ������ҵ�����г���ϡ�����ȥ����Ʒ��������⣬�÷�Ӧ�Ļ�ѧ����ʽΪ ��
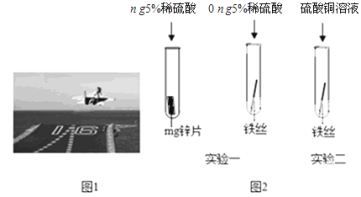
��3��Ϊ�˱����ִ��ĸ�����DZ���ʴ��ͨ�����ִ��������Ƕ�������ǿ������С��Ϊ̽��п������ͭ���ֽ����Ļ��˳���������ͼ2������ʵ�飺
��ʵ��һ�У�С���ԡ���������������ݵĿ�����Ϊ�����ж�п�����Ļ��ǿ������ͬѧ��Ϊ���������������� ��
��ʵ����У������� ����֤�����Ļ��ǿ��ͭ���÷�Ӧ�Ļ�ѧ����ʽΪ ��
���𰸡���1�������ᣬǿ�ȴ�
��2��H2O��O2 Fe2O3 + 6HCl==FeCl3 + 3H2O
��3��������Ӵ��������ͬ ����˿�����к�ɫ�����۳� Fe + CuSO4==Cu + FeSO4
��������
�����������1�����Ͻ���������ɻ�����ǣ����Ͻ���ʵ���Ҫ�ŵ����������ᣬǿ�ȴ�������ʴ��ǿ�� ��2����������ʴ��Ҫ����������е�H2O��O2��ͬ���õĽ�����������Ҫ�ɷ���������������ϡ�����ȥ����Ʒ��������⣬��Ӧ�Ļ�ѧ����ʽΪ��Fe2O3 + 6HCl==FeCl3 + 3H2O
��3����Ҫ̽��п������ͭ���ֽ����Ļ��˳����һ��Ҫע����Ƶ�һ������ʵ��һ�У�С���ԡ���������������ݵĿ�����Ϊ�����ж�п�����Ļ��ǿ������ͬѧ��Ϊ��������������������Ӵ��������ͬ��һ���õ���пƬ��һ���õ�����˿
��ʵ����У���������˿�����к�ɫ�����۳�����֤�����Ļ��ǿ��ͭ����Ӧ�Ļ�ѧ����ʽΪ�� Fe + CuSO4==Cu + FeSO4