题目内容
有A、B、C、D四种元素,其核电荷数在1至20之间,B原子和D原子的核外电子总数分别等于他们各自的电子层数的4倍,这两种元素能形成DB型的化合物,B元素在化合物中显负价,A原子和D原子的核外电子层数相同,A元素能和C元素形成CA型化合物,并知CA的溶液能与锌反应产生氢气,C元素的原子质量和体积在所有元素的原子中最小.试推断:
(1)写出A、B、C、D的元素的符号;
A
(2)写出C的单质在空气中燃烧生成的化合物的化学式;
(3)写出D的阳离子与A的阴离子的结构示意简图以及它们所形成的化合物的化学式.
(1)写出A、B、C、D的元素的符号;
A
Cl
Cl
BO
O
CH
H
DMg
Mg
;(2)写出C的单质在空气中燃烧生成的化合物的化学式;
(3)写出D的阳离子与A的阴离子的结构示意简图以及它们所形成的化合物的化学式.
分析:依据C元素的原子质量和体积在所有元素的原子中最小可知C是氢元素,并知CA的溶液能与锌反应产生氢气,说明CA是HCl,所以A是氯元素,A原子和D原子的核外电子层数相同,所以D的电子层数是3层,D原子的核外电子总数分别等于他们各自的电子层数的4倍,所以可知该元素原子的核外共有12个电子,则其核内有12个质子,为镁元素;以此结合题干中的信息分析解答即可;
解答:解:因为C元素的原子质量和体积在所有元素的原子中最小可知C是氢元素,并知CA的溶液能与锌反应产生氢气,说明CA是HCl,所以A是氯元素,A原子和D原子的核外电子层数相同,所以D的电子层数是3层,D原子的核外电子总数分别等于他们各自的电子层数的4倍,所以可知该元素原子的核外共有12个电子,则其核内有12个质子,为镁元素;由于有A、B、C、D四种元素,其核电荷数在1至20之间,B原子和D原子的核外电子总数分别等于他们各自的电子层数的4倍,所以B核外一定存在两个电子层,且核外存在8个电子,则其核内有8个质子,为氧元素;
(1)由以上分析可知A、B、C、D的元素的符号分别为:Cl;O;H;Mg;
(2)C的单质是氢气在空气中燃烧生成的化合物是水其化学式为:H2O;
(3)根据D的最外层电子数是2,化学反应中易失掉最外层的两个电子而带两个单位的正电荷,其结构示意图为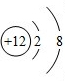 ;而A的原子最外层电子数是7,化学反应中易得到一个电子而带一个单位的负电荷,其结构示意图为
;而A的原子最外层电子数是7,化学反应中易得到一个电子而带一个单位的负电荷,其结构示意图为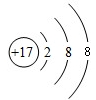 所以两者形成化合物的化学式为MgCl2;
所以两者形成化合物的化学式为MgCl2;
故答案为:(1)Cl;O;H;Mg;(2)H2O;(3)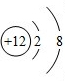 ;
; ;MgCl2;
;MgCl2;
(1)由以上分析可知A、B、C、D的元素的符号分别为:Cl;O;H;Mg;
(2)C的单质是氢气在空气中燃烧生成的化合物是水其化学式为:H2O;
(3)根据D的最外层电子数是2,化学反应中易失掉最外层的两个电子而带两个单位的正电荷,其结构示意图为
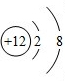 ;而A的原子最外层电子数是7,化学反应中易得到一个电子而带一个单位的负电荷,其结构示意图为
;而A的原子最外层电子数是7,化学反应中易得到一个电子而带一个单位的负电荷,其结构示意图为 所以两者形成化合物的化学式为MgCl2;
所以两者形成化合物的化学式为MgCl2;故答案为:(1)Cl;O;H;Mg;(2)H2O;(3)
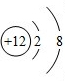 ;
; ;MgCl2;
;MgCl2;点评:此题是对元素种类的推断题,解题的关键是利用原子的核外电子排布情况对元素种类进行分析推断;

练习册系列答案
相关题目