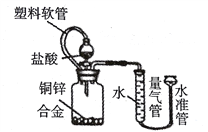
题目内容
【题目】一包混有杂质的Na2CO3,其杂质可能是Ba(NO3)2、KCl、NaHCO3中的一种或几种,今取10.6g样品,溶于水得到澄清的溶液,另取10.6g样品,加入足量的盐酸,完全反应生成4.4gCO2,则下列判断正确的是()
A. 样品中只含有杂质NaHCO3 B. 样品中不含杂质KCl
C. 样品中杂质为NaHCO3、Ba(NO3)2 D. 样品中杂质为KCl和NaHCO3
【答案】D
【解析】混有杂质的碳酸钠加水后溶液澄清,一定不存在Ba(NO3)2;纯净的碳酸钠10.6克时,会生成二氧化碳4.4克,纯净的碳酸氢钠10.6克生成的二氧化碳为: ![]() >4.4g,KCl的不与盐酸反应生成二氧化碳,会导致生成的二氧化碳的量偏小;现在取10.6克样品,加入足量的盐酸,收集到4.4gCO2,说明碳酸钠中的杂质与盐酸反应生成的二氧化碳与碳酸钠与盐酸反应的情况相同,则混合液物中一定存在KCl和NaHCO3,故选D。
>4.4g,KCl的不与盐酸反应生成二氧化碳,会导致生成的二氧化碳的量偏小;现在取10.6克样品,加入足量的盐酸,收集到4.4gCO2,说明碳酸钠中的杂质与盐酸反应生成的二氧化碳与碳酸钠与盐酸反应的情况相同,则混合液物中一定存在KCl和NaHCO3,故选D。

【题目】小明选择“铝丝和盐酸反应的快慢与什么因素有关”的课题开展探究。下表是他分别用相同质量的铝丝和足量稀盐酸反应的三组实验数据:
实验编号 | 盐酸的浓度/% | 反应温度/℃ | 铝丝消失 的时间/s |
① | 3 | 20 | 500 |
② | 6 | 20 | 300 |
③ | 6 | 30 | 80 |
(1)写出铝和盐酸反应的化学方程式:________________________________。
(2)实验②和③表明:该反应的快慢与__________有关。
(3)能表明盐酸浓度对反应快慢有影响的实验编号是________和________。
(4)如果把实验①中盐酸的浓度改为4%,请你推出铝丝消失的时间(用t表示)的取值范围:________________。
(5)该实验除了用铝丝消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量该反应的快慢吗?
方法:_____________________________________________________________________。
【题目】过氧化纳(化学式为Na2O2)可用在呼吸面具中作为氧气来原, Na2O2能和CO2反应生成O2和另—种固体化合物 (用x表示)。
【掲出猜想】有同学猜想X可能是酸,碱性盐中的一种,通过对物质组成的分析大家一致认为X肯定不是酸和碱,理由是__________.
【设计方案】请完成下表
实验步骤 | 实验现象 | 实验结论 |
实验一:取少量X,滴加稀盐酸.将产生的气体通入澄清石灰水 | 有气泡产生___________ | X为Na2CO3 |
实验二.取少量 X,加水配成溶液, 滴加的溶液.该碱可是______ | 生成白色沉淀 |
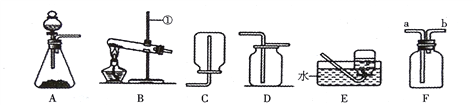
【拓展探究】用下图所示装置进行二氧化与过氧化钠(Na2O2)的反应。
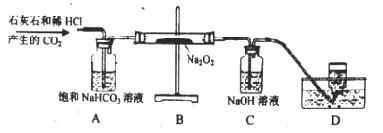
(1)装置A的作用是吸收CO2中混有的HCl, 装置C中反应的化学方程___________
(2)测量装置D中收集的气体体积,可用下图中的__________进行收集。
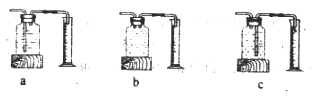
(3)兴趣小组查阅资料发现Na2O2也用H2O反应生成NaOH和O2为探究反应后装置B中固体的成分,甲同学取固体于试管中,加足量水,无气抱产生,则固体中—定没有________将所得溶液分成两份,进行下表所示实验:
实验操作 | 实验现象 | 分析与结论 |
向一份溶液中滴加过量的稀HCL | 有气泡产生 | B中固体有Na2CO3 |
向另一份溶液中_____ | 溶液变红 | B中固体有NaOH |