题目内容
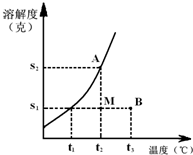 某固体物质的溶解度曲线如图所示,根据图回答如下问题:
某固体物质的溶解度曲线如图所示,根据图回答如下问题:(1)图中B点的意义:表示该物质在t3℃时,每100g溶剂和S1g溶质形成不饱和溶液.A点的意义:
表示该物质在t2℃时,每100g溶剂和S2g溶质形成饱和溶液
表示该物质在t2℃时,每100g溶剂和S2g溶质形成饱和溶液
.此溶液的溶质质量分数的表达式W(B)═[S2/(100+S2)]×100%
W(B)═[S2/(100+S2)]×100%
.(2)若A、B两点的溶液在保持温度不变的情况下各加20克水,A点的溶解度将
不变
不变
(填“增大”、“减小”、或“不变”);A、B的溶质质量分数前者大
前者大
(填“前者大”、“后者大”或“相等”).(3)当温度降低时,A点变动后溶液的质量分数与原来比较
减小
减小
(填“增大”、“减小”或“不变”).(4)若使M点的(100+S1)g溶液成为饱和溶液的方法:降温至
t1
t1
℃;增加溶质S2-S1
S2-S1
g和蒸发溶剂
蒸发溶剂
.分析:(1)由固体物质的溶解度曲线图,则可知A点的意义;可求A点溶液的溶质质量分数;
(2)溶解度为物质在某一温度时的溶解能力,故是否加水,不会影响溶解度大小;质量分数变化;
(3)由图可知,温度越高溶解的物质越多,浓度越大,反之越小;
(4)掌握不饱和溶液变为饱和溶液的方法.
(2)溶解度为物质在某一温度时的溶解能力,故是否加水,不会影响溶解度大小;质量分数变化;
(3)由图可知,温度越高溶解的物质越多,浓度越大,反之越小;
(4)掌握不饱和溶液变为饱和溶液的方法.
解答:解:(1)图中B点的意义:表示该物质在t3℃时,每100g溶剂和S1g溶质形成不饱和溶液.A点的意义:表示该物质在t2℃时,每100g溶剂和S2g溶质形成饱和溶液.此溶液的溶质质量分数的表达式 W(B)═[S2/(100+S2)]×100%;
(2)若A、B两点的溶液在保持温度不变的情况下各加20克水,A点的溶解度将不变;A、B的溶质质量分数 前者大;
(3)由图可知,温度越高溶解的物质越多,浓度越大,反之越小;故当温度降低时,A点变动后溶液的质量分数与原来比较 减小.
(4)若使M点的(100+S1)g溶液成为饱和溶液的方法:降温至 t1℃;增加溶质 S2-S1g和 蒸发溶剂.
故答案为:(1)表示该物质在t2℃时,每100g溶剂和S2g溶质形成饱和溶液.
W(B)═[S2/(100+S2)]×100%
(2)不变,前者大.(3)减小.(4)t1;S2-S1;蒸发溶剂
(2)若A、B两点的溶液在保持温度不变的情况下各加20克水,A点的溶解度将不变;A、B的溶质质量分数 前者大;
(3)由图可知,温度越高溶解的物质越多,浓度越大,反之越小;故当温度降低时,A点变动后溶液的质量分数与原来比较 减小.
(4)若使M点的(100+S1)g溶液成为饱和溶液的方法:降温至 t1℃;增加溶质 S2-S1g和 蒸发溶剂.
故答案为:(1)表示该物质在t2℃时,每100g溶剂和S2g溶质形成饱和溶液.
W(B)═[S2/(100+S2)]×100%
(2)不变,前者大.(3)减小.(4)t1;S2-S1;蒸发溶剂
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.

练习册系列答案
相关题目
 下表为KNO3在不同温度时的溶解度;
下表为KNO3在不同温度时的溶解度;
| 温度/°C | 0 | 20 | 40 | 60 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 |
(2)从溶解度曲可以看出,KNO3溶液的溶解度随温度的升高而________;若某固体物质的溶解度受温度的影响不大,这物质可能是________.
下表为KNO3在不同温度时的溶解度;
(1)请根据上表数据在图中画出 KNO3的溶解度曲线;
(2)从溶解度曲可以看出,KNO3溶液的溶解度随温度的升高而 ;若某固体物质的溶解度受温度的影响不大,这物质可能是 .

| 温度/°C | 20 | 40 | 60 | |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 |
(2)从溶解度曲可以看出,KNO3溶液的溶解度随温度的升高而 ;若某固体物质的溶解度受温度的影响不大,这物质可能是 .

 下表为KNO3在不同温度时的溶解度;
下表为KNO3在不同温度时的溶解度;