题目内容
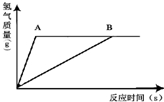 金属A、B跟质量相同、质量分数相同的稀硫酸反应,生成氢气的质量与反应时间有如图所示关系(已知:A、B在生成物中均为+2价).则下列结论中,不合理的是( )
金属A、B跟质量相同、质量分数相同的稀硫酸反应,生成氢气的质量与反应时间有如图所示关系(已知:A、B在生成物中均为+2价).则下列结论中,不合理的是( )分析:观察金属和酸溶液反应的图象,进行分析可以得出:①得到的氢气的多少②金属的活动性强弱:反应过程需要的时间越短说明该金属的活动性越强.
解答:解:A、由图象可知,反应结束后生成氢气的质量A=B,故A说法正确;
B、如果参加反应的金属均反应完,由于A、B在生成物中均显+2价,生成氢气的质量相等,那么相对原子质量A=B,故B说法错误;
C、由图象可知,相同的时间内,A放出的氢气多,说明了金属的活动性A>B,故C说法正确;
D、由图象可知,如果两种金属都有剩余,都把硫酸反应完,由于硫酸是质量相同、质量分数相同的稀硫酸,所以得到的氢气也能相等,故D说法正确.
故选B.
B、如果参加反应的金属均反应完,由于A、B在生成物中均显+2价,生成氢气的质量相等,那么相对原子质量A=B,故B说法错误;
C、由图象可知,相同的时间内,A放出的氢气多,说明了金属的活动性A>B,故C说法正确;
D、由图象可知,如果两种金属都有剩余,都把硫酸反应完,由于硫酸是质量相同、质量分数相同的稀硫酸,所以得到的氢气也能相等,故D说法正确.
故选B.
点评:主要考查了金属和酸溶液的反应的图象从中可以得到什么样的信息,从而培养学生分析问题、解决问题的能力,加强学生对金属活动性顺序的理解.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
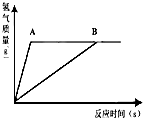 28、某课外活动小组为探究实验室制取氢气的方案,分别用金属A、B跟质量相同、质量分数相同的稀硫酸反应,经实验发现:生成氢气的质量与反应时间有如图所示关系.分析图象得到的以下结论中,不合理的是( )
28、某课外活动小组为探究实验室制取氢气的方案,分别用金属A、B跟质量相同、质量分数相同的稀硫酸反应,经实验发现:生成氢气的质量与反应时间有如图所示关系.分析图象得到的以下结论中,不合理的是( )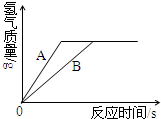 某小组为探究实验室制取氢气的方案,分别用等质量的金属A、B跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如图所示.分析图象得到的下列结论中,不合理的是(已知A、B在生成物中均显+2价)( )
某小组为探究实验室制取氢气的方案,分别用等质量的金属A、B跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如图所示.分析图象得到的下列结论中,不合理的是(已知A、B在生成物中均显+2价)( )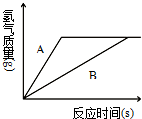 某课外活动小组为探究实验室制取氢气的方案,分别用金属A、B跟质量相同、质量分数相同的稀硫酸反应,经实验发现:生成氢气的质量与反应时间有如图所示关系.分析图象得到的以下结论中,不合理的是( )
某课外活动小组为探究实验室制取氢气的方案,分别用金属A、B跟质量相同、质量分数相同的稀硫酸反应,经实验发现:生成氢气的质量与反应时间有如图所示关系.分析图象得到的以下结论中,不合理的是( ) (2006?济宁)某课外活动小组为探究实验室制取氢气的方案,分别用金属A、B跟质量相同、质量分数相同的稀硫酸反应,经实验发现:生成氢气的质量与反应时间有下图所示关系.分析图象得到的以下结论中,不合理的是( )
(2006?济宁)某课外活动小组为探究实验室制取氢气的方案,分别用金属A、B跟质量相同、质量分数相同的稀硫酸反应,经实验发现:生成氢气的质量与反应时间有下图所示关系.分析图象得到的以下结论中,不合理的是( )