题目内容
【题目】根据下图回答有关问题。
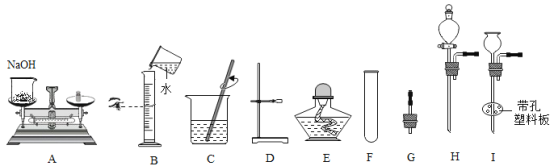
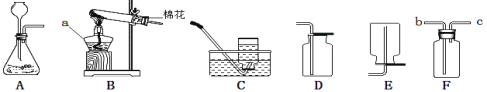
(1)仪器E的名称为_____。
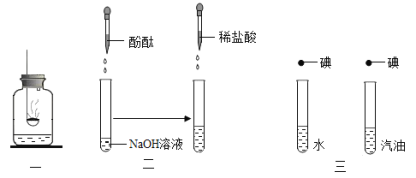
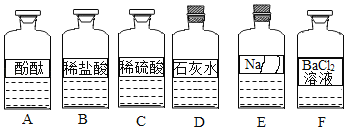
(2)图A~C是配制一定溶质质量分数 NaOH溶液中的三个步骤。其中有一个错误的操作,请指出并改正:_____;_____。
(3)选择仪器D~I完成下列实验操作:
①实验室用氯酸钾制取氧气的发生装置,应选仪器_____(填序号),其化学反应方程式为_____。
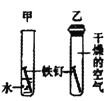
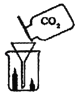
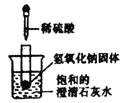
②实验室用电石(固体,主要成分CaC2)和水常温下反应制取乙炔(C2H2)气体,该反应极剧烈,发生装置应选仪器_____(填序号),该装置具有的优点是_____,利用上述装置还可以制取二氧化碳,请写出检验该气体的化学方程式_____。
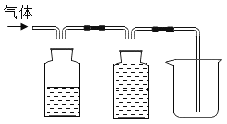
(4)用锌粒与稀盐酸制得的氢气中常混有酸性气体,为了得到较纯净的H2,可将气体通过_____(填试剂名称)洗气瓶后,用排水法收集,请在下图中将除杂及收集装置补画完整。_____
【答案】酒精灯 B 接近刻度线时要用胶头滴管滴加 DEFG 2KClO3![]() 2KCl+3O2↑ DFH 可以控制反应速率 CO2+Ca(OH)2=CaCO3↓+H2O 氢氧化钠溶液
2KCl+3O2↑ DFH 可以控制反应速率 CO2+Ca(OH)2=CaCO3↓+H2O 氢氧化钠溶液 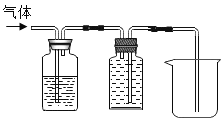
【解析】
本题主要考察实验室制取气体时发生装置和收集装置的选择
(1)仪器E的名称是酒精灯
(2)装置B操作错误;当量取准确液体体积时,最后需要用胶头滴管滴加,不能一直用烧杯加入液体。
(3)氯酸钾制氧气需要选择固体加热装置,铁架台、试管、酒精灯、单孔塞;反应原理:2KClO3![]() 2KCl+3O2↑;实验室用电石和水常温下反应制取乙炔(C2H2)气体,该反应极剧烈,选择固、液发生装置,同时需要控制反应速率,选择的装置有:铁架台、试管、分液漏斗(带双孔塞、玻璃导管);分液漏斗可以控制加入药品的质量,从而控制反应速率;实验室检验二氧化碳气体的原理,将气体通入澄清的石灰水:CO2+Ca(OH)2=CaCO3↓+H2O
2KCl+3O2↑;实验室用电石和水常温下反应制取乙炔(C2H2)气体,该反应极剧烈,选择固、液发生装置,同时需要控制反应速率,选择的装置有:铁架台、试管、分液漏斗(带双孔塞、玻璃导管);分液漏斗可以控制加入药品的质量,从而控制反应速率;实验室检验二氧化碳气体的原理,将气体通入澄清的石灰水:CO2+Ca(OH)2=CaCO3↓+H2O
(4)氢氧化钠碱性溶液可以吸收氯化氢酸性气体;洗气装置气体选择“长管进、短管出”,排水法收集气体时选择“短管进、长管出”如图: