题目内容
【题目】(4.5分)元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是依据元素周期表画出的1~18号元素的原子结构示意图。我对它进行研究:
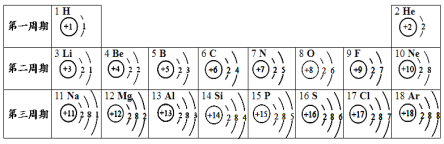
(1)原子序数为16的元素名称是 ,在化学反应中,该元素的原子容易 电子,变成 (填符号);原子序数为11的元素属于 (填“金属”或“非金属”)元素。
(2)根据图示信息,推测一个一氧化碳分子中所含的电子总数为 。
(3)我发现如下规律:①原子最外层电子数一般不超过8个;
②金属元素的原子最外层电子数一般少于4个,非金属元素的原子原子最外层电子数一般多于4个;
③ ;
④ ;
(4)右图表示碘元素的 (填“原子”、“阳离子”或“阴离子”)结构示意图。由图 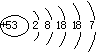 可知,碘元素应位于元素周期表中的第 周期。
可知,碘元素应位于元素周期表中的第 周期。
【答案】(1)硫 得到 S2- 金属 (2)14
(3)略(注:要突出规律,不能针对某一具体元素回答)
(4)原子 5
【解析】
试题分析:(1)元素符号前面的数字为原子序数,故原子序数为16的元素名称是硫;硫原子的最外层电子数为6,在化学反应中容易得到2个电子形成稳定结构;原子序数为11的是钠元素,钠元素属金属元素;
(2)一个一氧化碳分子是由一个碳原子和1个氧原子构成的,一个碳原子的电子数为6,一个氧原子的电子数为8,故一氧化碳分子中的电子数为14;
(3)同一周期的原子的电子层数相同,最外层电子数逐渐增加;
(4)该结构示意图中质子数=核外电子数,故属于原子;碘原子有5个电子层,属于第五周期。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案【题目】每空1分,共6分)某校化学兴趣小组就空气中氧气的含量进行实验探究:
【集体讨论】(1) 讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体。他们应该选择
A.蜡烛 B.红磷 C.硫粉
(2)为了充分消耗容器中的氧气,药品的用量应保证 。
(3)小组同学共同设计了如右图的两套装置,你认为合理的是(填字母) 。
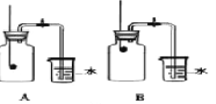
(4)为了确保实验的成功,在装药品之前应该 。
【分组实验】 在讨论的基础上,他们分组进行了实验。
【数据分析】实验结束后,整理数据如下:(注:集气瓶容积为100 mL)
组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入集气瓶中水的体积(mL) | 20 | 21 | 19 | 20 | 22 | 18 |
(5)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的 。
(6)通过实验还可以推断集气瓶中剩余气体的性质是 。