题目内容
【题目】常温下,铜制品生锈可生成绿色的铜绿。兴趣小组同学进行了下列相关探究。
探究一:甲组同学设计并进行实验,探究铜片生锈的必要条件。
【猜想】常温下,铜生锈可能与氧气、二氧化碳、水蒸气有关。
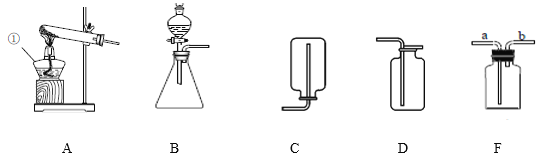
【实验】利用下图所示装置进行实验,并持续观察一个月。

他们观察到只有实验①中铜片表面生锈,实验②、③、④中铜片始终无明显变化。
【解释与结论】
(1)试管中的蒸馏水要预先煮沸,其目的是___________________________。
(2)实验④中氢氧化钠溶液的作用是____________________(用化学方程式表示)。
(3)得出“铜生锈一定与二氧化碳有关”的结论,依据的两个实验是________(填序号)。
(4)由上述实验推知,铜生锈的条件是与氧气、水蒸气、二氧化碳同时接触。
【反思与评价】
(5)在做猜想与假设时,同学们认为铜生锈与氮气无关,其理由是_________。
(6)欲进一步证明铜绿中含有碳酸盐,所需的试剂是________________。
探究二:乙组同学探究加热铜绿会生成什么物质。
他们与老师一起进行了下图所示的实验。实验过程中,观察到试管口有无色液体产生,澄清石灰水变浑浊。实验完成后,试管内固体由绿色变为黑色。
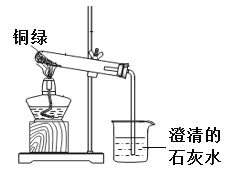
(7)他们经过讨论,猜想黑色固体可能是氧化铜或者是炭粉,或者是二者的混合物。乙组同学继续实验,取少量黑色固体于试管中,____________(填实验操作以及现象),证明只有氧化铜。写出该反应的化学方程式___________________。
【答案】 除去水中溶解的氧气和二氧化碳 2NaOH + CO2 = Na2CO3 + H2O ①④ 常温下氮气的化学性质不活泼,很难和其他物质反应 稀盐酸、澄清的石灰水 加入足量稀硫酸(或稀盐酸),黑色固体逐渐消失,溶液变成蓝色 CuO + H2SO4 = CuSO4 + H2O(或 CuO + 2HCl= CuCl2 + H2O)
【解析】常温下,铜制品生锈可生成绿色的铜绿。探究一:甲组同学设计并进行实验,探究铜片生锈的必要条件。【猜想】常温下,铜生锈可能与氧气、二氧化碳、水蒸气有关。【实验】利用下图所示装置进行实验,并持续观察一个月。他们观察到只有实验①中铜片表面生锈,实验②、③、④中铜片始终无明显变化。【解释与结论】(1)试管中的蒸馏水要预先煮沸,其目的是除去水中溶解的氧气和二氧化碳。(2)实验④中氢氧化钠溶液的作用是2NaOH + CO2 = Na2CO3 + H2O。(3)得出“铜生锈一定与二氧化碳有关”的结论,依据的两个实验是①④。(4)由上述实验推知,铜生锈的条件是与氧气、水蒸气、二氧化碳同时接触。【反思与评价】
(5)在做猜想与假设时,同学们认为铜生锈与氮气无关,其理由是. 常温下氮气的化学性质不活泼,很难和其他物质反应。(6)欲进一步证明铜绿中含有碳酸盐,所需的试剂是稀盐酸、澄清的石灰水。探究二:乙组同学探究加热铜绿会生成什么物质。下图所示的实验。实验过程中,观察到试管口有无色液体产生,澄清石灰水变浑浊。实验完成后,试管内固体由绿色变为黑色。(7)经过讨论,猜想黑色固体可能是氧化铜或者是炭粉,或者是二者的混合物。乙组同学继续实验,取少量黑色固体于试管中,加入足量稀硫酸(或稀盐酸),黑色固体逐渐消失,溶液变成蓝色。 证明只有氧化铜。该反应的化学方程式是CuO + H2SO4 = CuSO4 + H2O(或 CuO + 2HCl= CuCl2 + H2O)。
点睛∶本题主要考查探究铜片生锈的必要条件以及加热铜绿会生成什么物质。

 阅读快车系列答案
阅读快车系列答案