��Ŀ����
����Ŀ��ij��ѧ�С���ͬѧ�����ڽ�����ͼ��ʾ̽��ʵ�飬��ش����⣺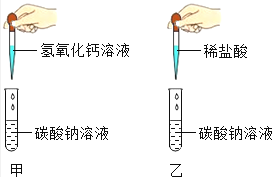
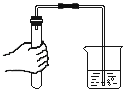
��1�����Թ����ܹ۲쵽��ʵ�������ǣ�
��2����Ӧ������ͬѧ�ǽ����ԹܵĄ�������ˣ�������Һ�����Թܷ�Һ����ͬһ����Һ���У��۲쵽�а�ɫ�����������ɴ˿�֪�����Թ�������Ϊ�� �� ���Թ�������Ϊ �� ����Һ�������ʽ��й�Һ���룬�õ���ҺW��
��3����������⡿��ҺW��һ��������Щ���ӣ����ܺ�����Щ���ӣ�
��ҺW��һ�����е��������������ӷ��ţ���
��4������������衿
���ܺ��е������ǣ�
Aͬѧ�����ܺ���CO32�� Bͬѧ�����ܺ���Ca2+Cͬѧ�����ܺ���H+
���һ����Ϊ��ͬѧ�IJ����Ǵ���ģ������Ǣ�
��5����ʵ��̽����
AͬѧΪ����֤�Լ��IJ��룬ȡ������ҺW���Թ��У������еμ�����ϡ���ᣬ�ߵ� ����û�й۲쵽���Ե�ʵ���������ǵó����ۣ��Լ��IJ��������ҺW�в���CO32�� �� BͬѧҲ��ϡ�������ʵ�飬ȴ�۲쵽�����Ե�ʵ���������ǵó����ۣ�Aͬѧ�IJ�����ȷ����ҺW�к���CO32��
�������뽻����
A��B��λͬѧ����ҩƷ��ͬ������ȴ��ͬ��ԭ������
��6�����ܽ�����ɡ���ʵ�鎡�����ǵ���ʾ��֤��ij�����Ӵ��ڵĹؼ��� ��
���𰸡�
��1����������
��2���������ơ��������ƣ��Ȼ��ơ�̼����
��3��Na+ Cl�� OH��
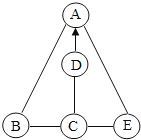
��4��̼������ӣ�������ӣ�C�������Ӻ����������Ӳ��ܹ���
��5��Aͬѧ�μӵ��������������������Ʒ�Ӧ�������������ұ��������ƺľ���Bͬѧ�μ�ϡ�������������������Ʒ�Ӧ������̼���Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼
��6�������������ʵ����Լ�
���������⣺��1�����Թ����ܹ۲쵽��ʵ�������Dz������ݣ�
����������ݣ���2����Ӧ������ͬѧ�ǽ����ԹܵĄ�������ˣ�������Һ�����Թܷ�Һ����ͬһ����Һ���У��۲쵽�а�ɫ����������˵�������������ƹ���������̼���ƹ�������˼��Թ��к���ʣ����������ƺͷ�Ӧ���ɵ��������ƣ����Թ��к���ʣ���̼���ƺͷ�Ӧ���ɵ��Ȼ��ƣ�����������ơ��������ƣ��Ȼ��ơ�̼���ƣ���3����ҺW��һ�����е������ǣ���Ӧ���ɵ����������е������Ӻ����������ӣ���Ӧ���ɵ��Ȼ����е������Ӻ������ӣ����Na+ Cl�� OH�� ��
����������衿
���ܺ��е�������̼������ӣ�������ӣ���̼���ƹ���ʱ������̼������ӣ����������ƹ���ʱ�����и����ӣ����̼������ӣ�������ӣ�
���һ����Ϊ��Cͬѧ�IJ����Ǵ���ģ������Ǣ������Ӻ����������Ӳ��ܹ��森
���C�������Ӻ����������Ӳ��ܹ��森�������뽻����
A��B��λͬѧ����ҩƷ��ͬ������ȴ��ͬ��ԭ����Aͬѧ�μӵ��������������������Ʒ�Ӧ�������������ұ��������ƺľ���
Bͬѧ�μ�ϡ�������������������Ʒ�Ӧ������̼���Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼��
���Aͬѧ�μӵ��������������������Ʒ�Ӧ�������������ұ��������ƺľ���
Bͬѧ�μ�ϡ�������������������Ʒ�Ӧ������̼���Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼��
���ܽ�����ɡ�
��ʵ�鎡�����ǵ���ʾ��֤��ij�����Ӵ��ڵĹؼ��Ǽ����������ʵ����Լ���
��������������ʵ����Լ���

 A�ӽ��� ϵ�д�
A�ӽ��� ϵ�д� ȫ�Ų��Ծ�ϵ�д�
ȫ�Ų��Ծ�ϵ�д�