题目内容
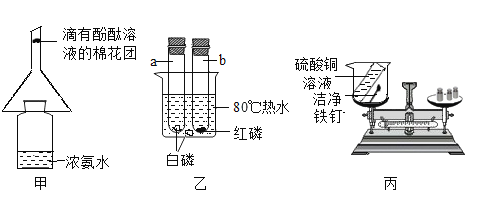
【题目】如图,甲、乙是酚酞溶液,丙是浓氨水,用大烧杯把甲、丙倒扣在里面。
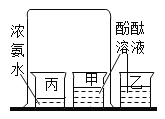
(1)实验过程中可以观察到_________________。
(2)通过你观察到的实验事实,通过分析、比较,可以得出与微粒性质有关的结论(写三条)___________。
【答案】甲烧杯中,溶液从无色逐渐变成红色,乙、丙烧杯溶液不变色 分子是不断运动的;不同的分子运动速率不同;氨分子比酚酞分子运动快(其他正确答案也给分)
【解析】
(1)实验过程中可以观察到甲烧杯中,溶液从无色逐渐变成红色,乙、丙烧杯溶液不变色。
(2)通过你观察到的实验事实,通过分析、比较,可以得出与微粒性质有关的结论是:分子是不断运动的;不同的分子运动速率不同;氨分子比酚酞分子运动快。

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
【题目】化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用2g石灰石样品,把20g稀盐酸(氯化氢的水溶液)分4次加入样品中(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、千燥等操作,最后称量,得实验数据如下:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入5.0g | 1.4g |
第二次加入5.0g | 0.8g |
第三次加入5.0g | 0.2g |
第四次加入5.0g | 0.2g |
(1)从以上数据可知,这四次实验中,第________________次石灰石样品中碳酸钙已完全反应,判断的依据是__________________。
(2)求该石灰石样品与稀盐酸反应产生的二氧化碳质量。______