题目内容
26.(6分)用下列仪器和试剂验证影响金属与盐酸反应速率的因素:烧杯、试管夹、酒精灯、药匙、量筒、天平。锌片、铁片、镁片。5%盐酸、20%盐酸。
(一)不同金属与酸反应的快慢不同
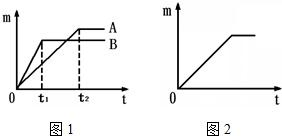
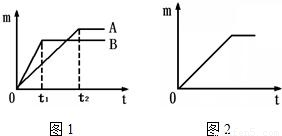
取质量相等的上述两种金属,分别放入溶质质量分数相同的足量稀盐酸中,
生成氢气的质量(m)与反应时间(t)的关系曲线如图1所示。
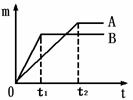
![]()
(1)金属活动性顺序表(填元素符号)
K、Ca、Na、 、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au
(2)线B对应的金属为 。
(3)线A对应的金属与稀盐酸反应的化学方程式 。
(二)金属与不同质量分数的盐酸反应的快慢不同
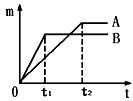
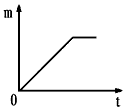
取质量相等的锌片,分别放入5%、20%的足量稀盐酸中。
生成氢气的质量为m,反应时间为t。5%的盐酸与锌片反应m与t的关系曲线如图2所示。请在该图上补画出20%的盐酸与锌片反应m与 t的关系曲线。
实验表明,盐酸质量分数越大,与金属反应的速率越快。
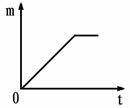
![]()
(三)温度对金属与盐酸反应速率也有影响
取两个烧杯,分别加入等质量的 (“同种”、 “不同种”)金属,再分别加入足量的质量分数 (“相同”、 “不相同”)的稀盐酸……实验表明,温度越高,盐酸与金属反应的速率越快。
(1)Mg、Al、Zn、Fe(全对得1分)
(2)Zn (3)Fe+2HCl= FeCl2+H2↑
(三)同种 相同


练习册系列答案
相关题目
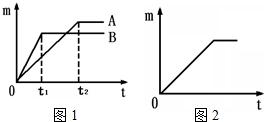 27、用下列仪器和试剂验证影响金属与盐酸反应速率的因素:烧杯、试管夹、酒精灯、药匙、量筒、天平.锌片、铁片、镁片.5%盐酸、20%盐酸.
27、用下列仪器和试剂验证影响金属与盐酸反应速率的因素:烧杯、试管夹、酒精灯、药匙、量筒、天平.锌片、铁片、镁片.5%盐酸、20%盐酸.