题目内容
【题目】t1℃时,将等质量的硝酸钾和氯化钾分配加入到各盛有10g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示.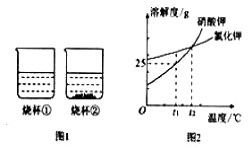
(1)烧杯①中溶解的溶质是(写名称或化学式);
(2)将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水g;
(3)关于图1中烧杯内的物质,下列说法正确的是 .
A.烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数
B.蒸发一定量的水,两烧杯中都一定有固体析出
C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
D.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)
【答案】
(1)KCl
(2)50
(3)A D
【解析】解:(1)在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。由图可知,t1℃时,硝酸钾的溶解度比氯化钾的小,烧杯①中溶解的溶质是氯化钾;(2)饱和溶液溶质的质量分数=溶解度÷(溶解度+100g)×100%,溶液的稀释过程中溶质的质量不变,将t1℃时,设50g硝酸钾的饱和溶液稀释成10%的溶液,需要水的质量为x, 50g× ![]() =(50g+x)×10%,x=50g;(3)图1中,两烧杯内溶剂相等,烧杯①内溶液中溶质的质量>烧杯②内上层清液中溶质的质量,所以烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数;蒸发一定量的水,烧杯②中一定有固体析出,烧杯①内不一定有固体析出;将两个烧杯中的溶液混合,充分搅拌后,烧杯中不一定还有剩余固体,可能刚好饱和,也可能混合后的溶液不饱和。将温度升高到t2℃,由于两种物质的溶解度相同,所以两烧杯内溶液中溶质的质量相同,质量分数相等。
=(50g+x)×10%,x=50g;(3)图1中,两烧杯内溶剂相等,烧杯①内溶液中溶质的质量>烧杯②内上层清液中溶质的质量,所以烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数;蒸发一定量的水,烧杯②中一定有固体析出,烧杯①内不一定有固体析出;将两个烧杯中的溶液混合,充分搅拌后,烧杯中不一定还有剩余固体,可能刚好饱和,也可能混合后的溶液不饱和。将温度升高到t2℃,由于两种物质的溶解度相同,所以两烧杯内溶液中溶质的质量相同,质量分数相等。
所以答案是:(1)KCl;(2)50;(3)A D。
【考点精析】掌握固体溶解度曲线及其作用和溶质的质量分数、溶解性和溶解度的关系是解答本题的根本,需要知道1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和);溶质质量分数 =溶质质量/溶液质量*100% ;溶解度=溶质质量/溶剂质量*100g (必须选取饱和溶液);溶液质量=溶质质量(克)+溶剂质量(克) ;对于饱和溶液,溶液质量分数w = S/(S+100);所以溶解度S = 100/(1/w-1).

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案