题目内容
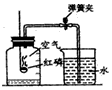
【题目】某初三兴趣小组同学利用下图装置进行了一系列实验。操作步骤如下:
(1)I.检查装置气密性:保持K1关闭,打开K2、K3 , 向乙中加水至浸没下端导管口,用热毛巾捂住甲瓶外壁,若观察到的现象,说明装置左侧气密性良好;用同样方法可以检查装置另一侧的气密性。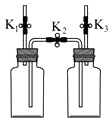
(2)II.向甲中加入石灰石,乙中加入碳酸钠溶液,连接装置。
III.打开K1 , 用注射器向甲中注入稀盐酸,直至页液面浸没下端导管口。
IV.通过K1上方导管收集气体(收集装置略去)。
V.打开K2、K3 , 关闭K1 , 最终观察到乙中溶液变浑浊,停止实验。
依据上述实验回答下列问题:
甲中发生的反应方程式为;乙中液体变浑浊的方程式。
(3)反应结束后,乙中溶质一定有 , 还有别的溶质吗?小组同学对此有如下猜想:
猜想一.没有别的溶质 猜想二.还有氯化钙
猜想三.还有氯化氢、氯化钙 猜想四.还有碳酸钠
其中,猜想不成立
为证明究竟哪种猜想正确,可以选择下列试剂中的(填字母)。
A.稀盐酸、碳酸钾溶液 B.碳酸钠溶液、氢氧化钡溶液
C.硝酸银溶液、稀硝酸 D.二氧化碳、稀盐酸
【答案】
(1)乙中的导管有气泡冒出
(2)CaCO3 + 2HCl=CaCl2 + CO2↑ + H2O,CaCl2+ Na2CO3=2NaCL +CaCO3↓
(3)NaCl,三,A
【解析】保持K1关闭,打开K2、K3,向乙中加水至浸没下端导管口,用热毛巾捂住甲瓶外壁,若观察到乙中的导管有气泡冒出的现象,说明装置左侧气密性良好;甲中发生的反应方程式为CaCO3 + 2HCl=CaCl2 + CO2↑ + H2O;乙中液体变浑浊的方程式CaCl2+ Na2CO3=2NaCL +CaCO3,反应结束后,乙中溶质一定有发生生成的氯化钠,猜想三不成立,因为如果有氯化氢则不会得到沉淀,加入盐酸会验证是否存在碳酸钠,加入碳酸钾可以验证是否存在氯化钙。
所以答案是:乙中的导管有气泡冒出;CaCO3 + 2HCl=CaCl2 + CO2↑ + H2O;CaCl2+ Na2CO3=2NaCL +CaCO3↓;NaCl;三;A
【考点精析】通过灵活运用检查装置的气密性,掌握装置气密性检查:先将导管的一端浸入水中,用手紧贴容器外壁,稍停片刻,若导管口有气泡冒出,松开手掌,导管口部有水柱上升,稍停片刻,水柱并不回落,就说明装置不漏气即可以解答此题.

【题目】某兴趣小组同学用下表所示的形式对所学物质进行分类(甲包含乙、丙)。其中正确的是
选项 | A | B | C | D |
甲 | 清洁能源 | 构成物质微粒 | 盐类 | 金属单质 |
乙、丙 | 氢气、石油 | 质子、中子 | 烧碱、纯碱 | 铜、汞 |
A. AB. BC. CD. D