题目内容
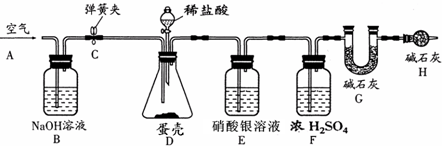
鸡蛋壳的成份主要是碳酸钙.将一新鲜的鸡蛋放在盛有足量稀盐酸的玻璃筒中,可观察到鸡蛋慢慢地上下浮动,好象在作“潜水运动”.解释这一现象________.
鸡蛋壳主要成分是碳酸钙,会与盐酸反应产生气体,蛋壳表面的气体推动鸡蛋上浮,当浮出液面一定程度时,气体逸出,鸡蛋的重力大于浮力,鸡蛋又将下沉.反复这样,就会看到鸡蛋“潜水运动”.
分析:碳酸钙能与盐酸反应生成二氧化碳气体,气体的存在能影响鸡蛋所受的浮力.
解答:鸡蛋壳的主要成分是碳酸钙,碳酸钙能与盐酸反应生成二氧化碳气体,生成的二氧化碳气体附在蛋壳表面,使鸡蛋受的浮力增大,会上浮,气体聚成大气泡离开蛋壳,则所受的浮力减小,会下降.
故答案为:鸡蛋壳主要成分是碳酸钙,会与盐酸反应产生气体,蛋壳表面的气体推动鸡蛋上浮,当浮出液面一定程度时,气体逸出,鸡蛋的重力大于浮力,鸡蛋又将下沉.反复这样,就会看到鸡蛋“潜水运动”.
点评:本题结合物理知识考查了碳酸钙与酸的反应,完成此题,可以依据已有的知识进行.
分析:碳酸钙能与盐酸反应生成二氧化碳气体,气体的存在能影响鸡蛋所受的浮力.
解答:鸡蛋壳的主要成分是碳酸钙,碳酸钙能与盐酸反应生成二氧化碳气体,生成的二氧化碳气体附在蛋壳表面,使鸡蛋受的浮力增大,会上浮,气体聚成大气泡离开蛋壳,则所受的浮力减小,会下降.
故答案为:鸡蛋壳主要成分是碳酸钙,会与盐酸反应产生气体,蛋壳表面的气体推动鸡蛋上浮,当浮出液面一定程度时,气体逸出,鸡蛋的重力大于浮力,鸡蛋又将下沉.反复这样,就会看到鸡蛋“潜水运动”.
点评:本题结合物理知识考查了碳酸钙与酸的反应,完成此题,可以依据已有的知识进行.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目