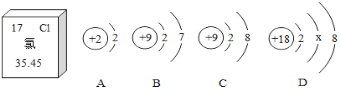题目内容
【题目】兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验。请你与他们 一起完成以下探究活动:
(对固体猜想)
猜想Ⅰ:全部是 NaOH;猜想Ⅱ:全部是 Na2CO3;猜想Ⅲ:是 NaOH 和 Na2CO3 混合物。
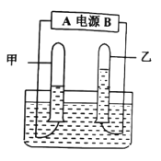
(实验和推断)取 11 克样品进行实验
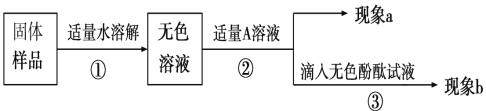
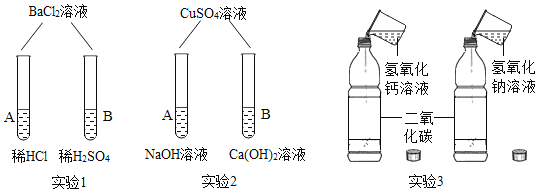
(1)若现象 a 为有气泡产生,说明氢氧化钠已经变质,有气泡产生的反应的化学方程式是_____________ ;
(2)若 A 是 Ca(OH)2 溶液,现象 a 有白色沉淀,现象 b 为无色酚酞试液变红色,该实验 ______ (填“能或不 能”)说明样品中有 NaOH,说明理由_______________________________;
(3)若 A 是 CaCl2 溶液,当实验现象 a 为产生白色沉淀,现象 b 为 _____,则猜想Ⅲ成立。 反应充分后,将现象 a 处的白色沉淀低温烘干,称其质量为 10g,请计算样品中碳酸钠的质量分数。_________(写 出计算过程)
(反思)久置的氢氧化钠变质的原因是(用化学方程式表示) _____
【答案】![]() 或
或![]() 不能 氢氧化钙能和碳酸钠反应生成氢氧化钠 溶液变红色 无答案
不能 氢氧化钙能和碳酸钠反应生成氢氧化钠 溶液变红色 无答案 ![]()
【解析】
实验和推断:
(1)若现象a为有气泡产生,说明氢氧化钠已经变质,有气泡产生,是因为碳酸钠和加入的稀盐酸或稀硫酸反应生成了二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑,Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;
(2)若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,该实验不能说明样品中有NaOH,理由是氢氧化钙能和碳酸钠反应生成氢氧化钠,影响对氢氧化钠的检验;
(3)若A是CaCl2溶液,当实验现象a为产生白色沉淀,说明溶液中含有碳酸钠,现象b为溶液变红色,说明溶液中含有氢氧化钠,则猜想Ⅲ成立;
设:碳酸钠质量为x。
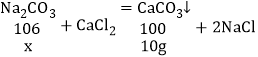
![]() x=10.6g,
x=10.6g,
样品中碳酸钠的质量分数=![]()
答:样品中碳酸钠的质量分数为96.4%。
反思:久置的氢氧化钠变质的原因是和二氧化碳反应生成了碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O。

 小学教材全测系列答案
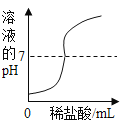
小学教材全测系列答案【题目】下列图像不能正确反映其对应操作的是
A | B | C | D |
|
|
|
|
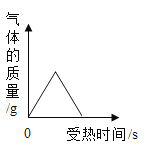
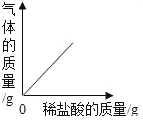
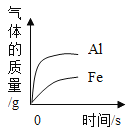
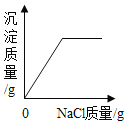
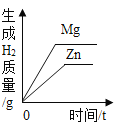
在一定量的AgNO3溶液中逐滴加入NaCl溶液 | 等质量Zn和Mg分别与足量的等浓度稀硫酸反应 | 向NaOH溶液中逐滴加入稀盐酸 | 等质量CaCO3分别与足量的等浓度稀盐酸反应 |
A. A B. B C. C D. D
【题目】化学学科实践活动课上,老师拿来一包粉末。它是由长期放置在空气中的铁粉和久置的碱石灰干燥剂混合而成,让同学们设计实验进行探究。
(提出问题)固体样品的成分是什么?
(查阅资料)(1)碱石灰干燥剂是CaO和NaOH的混合物。(2)CaCl2溶液显中性。
(猜想与假设)固体样品中可能含有 Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和_____等七种物质。
(进行实验)
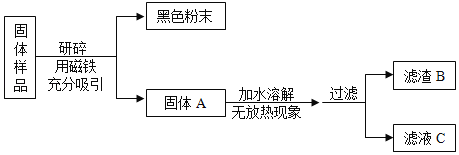
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 | 实验现象 | 实验结论及化学方程式 |
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 | ①_______________ ②_______________ | 结论:滤渣B中有 Fe2O3,CaCO3。 实验操作中Fe2O3与稀盐酸反应的化学方程式为:____________________ |
乙组同学对滤液C的成分进行探究,记录如下:
实验操作 | 实验现象 | 实验结论及化学方程式 |
取少量滤液C于试管中,加入过量CaCl2溶液,静置,向上层清液中滴加无色酚酞试液,振荡 | ①有白色沉淀生成 ②酚酞试液由无色变成红色 | 滤液C中有__________; 滤液C中的物质与CaCl2反应的化学方程式是_________________ |
(解释与结论)(1)乙组同学实验中加入过量CaCl2溶液的目的是________________________
(2)通过以上实验探究,该固体样品中能确定一定含有的成分是___________________。