题目内容
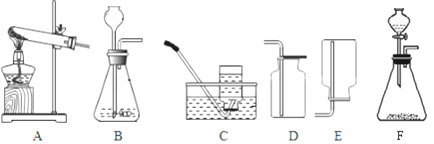
【题目】将50g稀盐酸10g大理石的烧杯中,恰好完全反应,烧杯中剩余物质的质量为57.8g(杂质不溶于水且不参加反应)求:
(1)生成CO2的质量______________;
(2)稀盐酸中溶质的质量分数__________;
(3)反应后所得溶液的质量分数__________。
【答案】2.2g 7.3% 10.5%
【解析】
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量。
解:(1)生成CO2的质量为:10g+50g-57.8g=2.2g;
(2)设稀盐酸中氯化氢质量为x,生成氯化钙质量为y,碳酸钙质量为z,
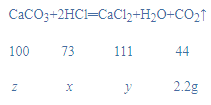
![]() x=3.65g,
x=3.65g,
![]() y=5.55g,
y=5.55g,
![]() z=5g,
z=5g,
稀盐酸中溶质的质量分数为:![]() ×100%=7.3%,
×100%=7.3%,
(3)反应后所得溶液的质量分数为:![]() ×100%=10.5%。
×100%=10.5%。

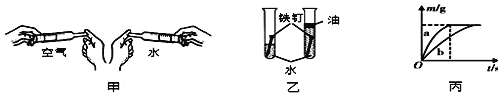
【题目】某化学兴趣小组根据下列转化关系在实验室中模拟炼铁,并对产物成分进行探究。
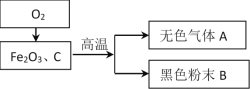
(1)炼铁的原理是______________________________(用化学方程式表示)。
(2)甲、乙两个兴趣小组分别对无色气体A和黑色粉末 B的成分进行探究。
(猜想与假设)
甲组在分析了炼铁的原理后,认为无色气体A中可能有CO2,也可能有未反应的_____。
乙组认为黑色粉末的成分中存在以下两种情况:
假设一:只含有铁。假设二:含有______________________________。
(实验探究)
①为验证甲组的猜想,同学们按下图所示装置进行实验(箭头表示气体流向)。
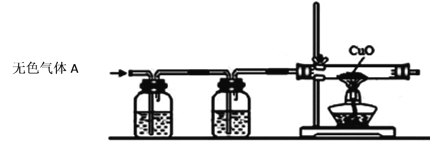
Ⅰ澄清石灰水Ⅱ浓硫酸Ⅲ氧化铜粉末
上述实验装置Ⅱ中浓硫酸的作用是吸收水蒸气,装置Ⅰ的作用是_______________,装置Ⅲ的作用是_________________。当看到Ⅰ中澄清石灰水变浑浊,Ⅲ中黑色固体变成红色后,可以确定无色气体A的成分是__________。
②为验证乙组中假设二是否成立,请你设计实验用化学方法完成以下探究。
实验方法 | 实验操作 | 实验现象 | 实验结论 |
化学方法 | _____ | _____ | 假设二成立 |
(交流反思)针对甲组实验存在的缺陷,同学们一起进行了改进,解决了污染环境问题。