题目内容
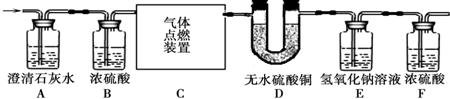
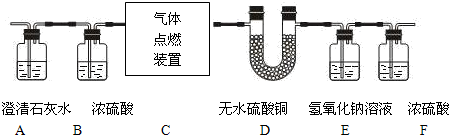
某无色气体中可能含有甲烷、一氧化碳、二氧化碳、氮气中的一种或几种,现将该气体依次通过下图所示装置,观察到:①A装置内未见有浑浊出现;②D装置内无水硫酸铜变蓝(无水硫酸铜遇水变蓝);最终收集到一定量干燥气体(假设每步反应都是完全的).请回答下列问题: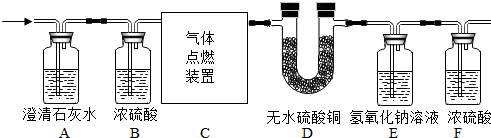
(1)由①可知原混合气体中肯定不含
(2)由②可知原混合气体中一定含有
(3)最终收集到的气体是
(4)实验过程中记录的实验数据如下:
| D装置总质量 | E、F装置总质量 | |
| 反应前 | 156.6g | 356.8g |
| 反应后 | 158.4g | 359.0g |
分析:(1)根据二氧化碳会与氢氧化钙反应生成碳酸钙沉淀进行分析,
(2)根据无水硫酸铜遇水变蓝的性质分析,
(3)根据ABCDEF各个步骤的作用和氮气的化学性质进行分析,
(4)根据各装置增加的质量求出碳氢元素的质量比和质量守恒定律进行分析.
(2)根据无水硫酸铜遇水变蓝的性质分析,
(3)根据ABCDEF各个步骤的作用和氮气的化学性质进行分析,
(4)根据各装置增加的质量求出碳氢元素的质量比和质量守恒定律进行分析.
解答:解:(1)二氧化碳通过澄清石灰水会生成碳酸钙沉淀,而本题混合气通过澄清石灰水没有现象,所以混合气中没有二氧化碳,故答案为:二氧化碳,
(2)无水硫酸铜遇水变蓝色,说明点燃后生成了水,根据质量守恒定律可知,原混合气中含有氢元素,故答案为:甲烷,
(3)根据(2)的推断,可知混合气中含有甲烷,假如也有一氧化碳,经过点燃后,甲烷和一氧化碳都转化成了水和二氧化碳,而氢氧化钠可以吸收二氧化碳,浓硫酸可以吸收水,最后只剩氮气了,故答案为:氮气,
(4)根据表中的数据可知,生成了水1.8克,二氧化碳2.2克,
H:
×1.8=0.2克
C:
×2.2=0.6克
碳氢原子个数比=
:
=1:4
所以该气体为甲烷.
可以确定经过点燃的是甲烷,故答案为:甲烷、氮气.
(2)无水硫酸铜遇水变蓝色,说明点燃后生成了水,根据质量守恒定律可知,原混合气中含有氢元素,故答案为:甲烷,
(3)根据(2)的推断,可知混合气中含有甲烷,假如也有一氧化碳,经过点燃后,甲烷和一氧化碳都转化成了水和二氧化碳,而氢氧化钠可以吸收二氧化碳,浓硫酸可以吸收水,最后只剩氮气了,故答案为:氮气,
(4)根据表中的数据可知,生成了水1.8克,二氧化碳2.2克,
H:
| 2 |
| 18 |
C:
| 12 |
| 44 |
碳氢原子个数比=
| 0.6 |
| 12 |
| 0.2 |
| 1 |
所以该气体为甲烷.
可以确定经过点燃的是甲烷,故答案为:甲烷、氮气.
点评:本题主要考查了根据装置中的现象推导混合气组成的方法,对混合气的检验要选用适当的试剂.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某无色气体中可能含有甲烷、一氧化碳、二氧化碳、氮气中的一种或几种,现将该气体依次通过下图所示装置,观察到:①A装置内未见有浑浊出现;②D装置内无水硫酸铜变蓝(无水硫酸铜遇水变蓝);③最终收集到一定量干燥气体(假设每步反应都是完全的).(已知浓硫酸可以干燥气体,氢氧化钠溶液可以吸收酸性气体)
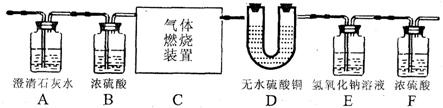
请回答下列问题:
(1)由①可知原混合气体中肯定不含 ;
(2)由③可知原混合气体中一定含有 ;
(3)最终收集到的气体是 (不包括过量氧气);
(4)实验过程中记录的实验数据如下:
则该气体的成分为: .

请回答下列问题:
(1)由①可知原混合气体中肯定不含
(2)由③可知原混合气体中一定含有
(3)最终收集到的气体是
(4)实验过程中记录的实验数据如下:
| D装置总质量 | E、F装置总质量 | |
| 反应前 | 156.6g | 356.8g |
| 反应后 | 158.4g | 361.2g |