题目内容
(2012?连云港一模)请你和小明一起进行实验室制取二氧化碳的探究.
(一)选择药品:小明对三组药品进行了研究,实验记录如下:
对照实验①②,是在探究不同的酸因素对制取二氧化碳气体产生影响;
对照实验①③,是在探究
小明选择第①组药品来制取二氧化碳,该组药品发生反应的化学方程式为
不选择第②组药品的原因是
(二)选择装置:
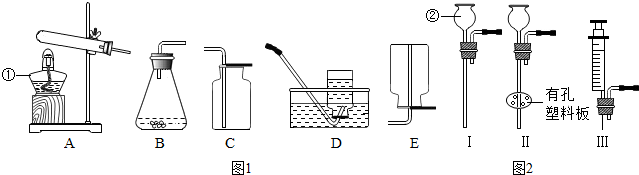
(1)写出图中带标号仪器的名称:①
(2)小明选择气体发生和收集的装置为
(3)气体检验:将生成的气体通入石蕊溶液中,溶液变红,请你写出反应的化学方程式
(4)装置B虽然操作简便,但无法控制反应速率.请从图2中选取
(一)选择药品:小明对三组药品进行了研究,实验记录如下:
| 组别 | 药 品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 粉末状石灰石和稀盐酸 | 产生气泡速率很快 |
对照实验①③,是在探究
石灰石形状
石灰石形状
因素对制取二氧化碳气体产生影响;小明选择第①组药品来制取二氧化碳,该组药品发生反应的化学方程式为
CaCO3+2HCl=CaCl2+CO2↑+H2O
CaCO3+2HCl=CaCl2+CO2↑+H2O
;不选择第②组药品的原因是
反应后生成硫酸钙微溶于水,覆盖在石灰石表面,使反应速度减慢并停止
反应后生成硫酸钙微溶于水,覆盖在石灰石表面,使反应速度减慢并停止
.(二)选择装置:

(1)写出图中带标号仪器的名称:①
酒精灯
酒精灯
、②长颈漏斗
长颈漏斗
.(2)小明选择气体发生和收集的装置为
B、C
B、C
请在A~E中选择),验满方法是C
C
.(3)气体检验:将生成的气体通入石蕊溶液中,溶液变红,请你写出反应的化学方程式
CO2+H2O=H2CO3
CO2+H2O=H2CO3
,因此他确定该气体是二氧化碳.他的检验方法是否正确?请说明理由不正确,其他酸性气体通入石蕊溶液中,溶液也变红
不正确,其他酸性气体通入石蕊溶液中,溶液也变红
.请你写出检验二氧化碳气体的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O
Ca(OH)2+CO2=CaCO3↓+H2O
.(4)装置B虽然操作简便,但无法控制反应速率.请从图2中选取
Ⅲ
Ⅲ
(填序号)取代B中的单孔塞,以达到控制反应速率的目的,起到随开随关的作用.分析:(一)这是一个对比实验,根据对比实验中的所选的药品的不同、实验现象的不同来探究各种因素对实验的影响;
(二)(1)根据实验室中的常见仪器用途与名称填空;
(2)实验室制取二氧化碳是“固体+液体”在常温下进行的实验,二氧化碳的密度比空气大,且溶于水,据此来选择气体的发生与收集装置;
(3)二氧化碳溶于水后生成弱酸H2CO3;酸性溶液都可以使紫色石蕊试液变红;二氧化碳可以使澄清的石灰水变浑浊.根据这三方面进行填空;
(4)要从控制反应速率和随开随关两个方面考虑.
(二)(1)根据实验室中的常见仪器用途与名称填空;
(2)实验室制取二氧化碳是“固体+液体”在常温下进行的实验,二氧化碳的密度比空气大,且溶于水,据此来选择气体的发生与收集装置;
(3)二氧化碳溶于水后生成弱酸H2CO3;酸性溶液都可以使紫色石蕊试液变红;二氧化碳可以使澄清的石灰水变浑浊.根据这三方面进行填空;
(4)要从控制反应速率和随开随关两个方面考虑.
解答:解:(一)对照实验①③所选的物品:它们所选的药品石灰石的形状不同,实验现象不同,由此可知,该实验是探究石灰石的形状对制取二氧化碳气体产生的影响.
石灰石与稀盐酸发生反应,生成氯化钙、水和二氧化碳气体.其反应方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O.
不选择第②组药品的原因是碳酸钙与硫酸反应,生成硫酸钙微溶于水,覆盖在石灰石表面,里面的石灰石不能与硫酸接触,使反应速度减慢并停止;
故填:石灰石形状;CaCO3+2HCl=CaCl2+CO2↑+H2O;反应后生成硫酸钙微溶于水,覆盖在石灰石表面,使反应速度减慢并停止;
(二)(1)图中①、②的仪器分别是酒精灯、长颈漏斗;
故填:①酒精灯,②长颈漏斗;
(2)制取二氧化碳用碳酸钙和盐酸,不需要加热,所以选择“固+液 常温型”的发生装置B,由于二氧化碳能溶于水,不能用排水法收集,密度比空气大只能用向上排空气法收集,故收集装置选择C;因为二氧化碳不燃烧,也不支持燃烧,所以验满方法是将燃着的木条放到集气瓶口,能够熄灭,说明已满;
故填:B、C;燃着木条伸到瓶口熄灭;
(3)二氧化碳溶于水后,生成弱酸碳酸,其反应方程式为:CO2+H2O=H2CO3.碳酸能使紫色石蕊试液变红,但是据此可以判定该气体是二氧化碳,这种说法是错误的,因为其他酸性气体通入石蕊溶液中,溶液也变红.一般情况下,根据二氧化碳能使澄清的石灰水变浑浊的特性,来检验二氧化碳的存在,其反应方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
故填:CO2+H2O=H2CO3;不正确,其他酸性气体通入石蕊溶液中,溶液也变红;Ca(OH)2+CO2=CaCO3↓+H2O;
(4)从控制反应速率和随开随关两个方面考虑,应该选择带注射器的,注射器可控制反应速度.故选Ⅲ.
石灰石与稀盐酸发生反应,生成氯化钙、水和二氧化碳气体.其反应方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O.
不选择第②组药品的原因是碳酸钙与硫酸反应,生成硫酸钙微溶于水,覆盖在石灰石表面,里面的石灰石不能与硫酸接触,使反应速度减慢并停止;
故填:石灰石形状;CaCO3+2HCl=CaCl2+CO2↑+H2O;反应后生成硫酸钙微溶于水,覆盖在石灰石表面,使反应速度减慢并停止;
(二)(1)图中①、②的仪器分别是酒精灯、长颈漏斗;
故填:①酒精灯,②长颈漏斗;
(2)制取二氧化碳用碳酸钙和盐酸,不需要加热,所以选择“固+液 常温型”的发生装置B,由于二氧化碳能溶于水,不能用排水法收集,密度比空气大只能用向上排空气法收集,故收集装置选择C;因为二氧化碳不燃烧,也不支持燃烧,所以验满方法是将燃着的木条放到集气瓶口,能够熄灭,说明已满;
故填:B、C;燃着木条伸到瓶口熄灭;
(3)二氧化碳溶于水后,生成弱酸碳酸,其反应方程式为:CO2+H2O=H2CO3.碳酸能使紫色石蕊试液变红,但是据此可以判定该气体是二氧化碳,这种说法是错误的,因为其他酸性气体通入石蕊溶液中,溶液也变红.一般情况下,根据二氧化碳能使澄清的石灰水变浑浊的特性,来检验二氧化碳的存在,其反应方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
故填:CO2+H2O=H2CO3;不正确,其他酸性气体通入石蕊溶液中,溶液也变红;Ca(OH)2+CO2=CaCO3↓+H2O;
(4)从控制反应速率和随开随关两个方面考虑,应该选择带注射器的,注射器可控制反应速度.故选Ⅲ.
点评:通过回答本题知道了对比实验的设计方法,掌握了实验室制取二氧化碳的反应原理和二氧化碳的验满方法,知道了能够控制反应速度的装置的选择方法.

练习册系列答案
相关题目
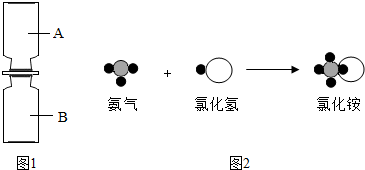 (2012?连云港一模)在化学晚会上,小军同学表演了一个化学小魔术“空瓶生烟”(如图1所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题:若用“
(2012?连云港一模)在化学晚会上,小军同学表演了一个化学小魔术“空瓶生烟”(如图1所示),A瓶中充满氯化氢气体,B瓶中充满氨气,抽开毛玻璃片,瓶中充满浓浓的白烟.请你根据所学知识回答下列问题:若用“ ”表示氢原子,用“
”表示氢原子,用“ ”表示氮原子,用“
”表示氮原子,用“ ”表示氯原子,上述反应过程可用图2表示.
”表示氯原子,上述反应过程可用图2表示.