题目内容
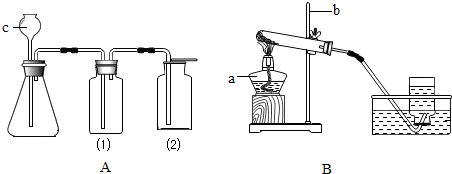
16、(1)氢氧化钠溶液长期暴露在空气中会逐渐变质,检验氢氧化钠溶液是否变质的试剂是
(2)如果要使氢氧化钠溶液的pH减小,可采取的方法有:
①不发生化学反应的方法
②有化学反应发生的其中一种方法(写化学反应方程式)
稀盐酸
,若已变质则检验时可观察到的现象是
有气泡产生
.(2)如果要使氢氧化钠溶液的pH减小,可采取的方法有:
①不发生化学反应的方法
加水
.②有化学反应发生的其中一种方法(写化学反应方程式)
NaOH+HCl═NaCl+H2O
.分析:(1)氢氧化钠容易吸收二氧化碳而变质,变质后生成碳酸钠,碳酸钠与酸反应产生二氧化碳气体;
(2)氢氧化钠溶液PH的大小与氢氧根离子的浓度有关,浓度越大,PH越大,要使氢氧化钠溶液的pH减小,就是降低氢氧根离子的浓度.
(2)氢氧化钠溶液PH的大小与氢氧根离子的浓度有关,浓度越大,PH越大,要使氢氧化钠溶液的pH减小,就是降低氢氧根离子的浓度.
解答:解:(1)氢氧化钠容易吸收二氧化碳而变质,变质后生成碳酸钠,要检验是否变质,就是检验是否含有碳酸钠,也就是碳酸盐的检验,碳酸盐与酸反应生成气体,所以本题答案为:稀盐酸,有气泡产生;
(2)氢氧化钠溶液PH的大小与氢氧根离子的浓度有关,浓度越大,PH越大,要使氢氧化钠溶液的pH减小,就是降低氢氧根离子的浓度,物理方法可以加水稀释,化学方法可以让氢氧化钠与酸发生中和反应,所以本题答案为:①加水,②NaOH+HCl═NaCl+H2O.
(2)氢氧化钠溶液PH的大小与氢氧根离子的浓度有关,浓度越大,PH越大,要使氢氧化钠溶液的pH减小,就是降低氢氧根离子的浓度,物理方法可以加水稀释,化学方法可以让氢氧化钠与酸发生中和反应,所以本题答案为:①加水,②NaOH+HCl═NaCl+H2O.
点评:本题可以以检验碳酸盐的存在作为解题的依据,还要明确溶液中氢离子或氢氧根离子的浓度与溶液PH的关系.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目

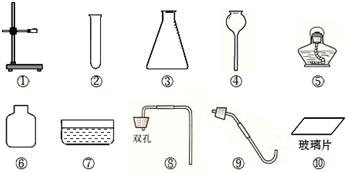 26、实验室提供了以下仪器,请你随某兴趣小组的同学一起来参加实验探究活动:
26、实验室提供了以下仪器,请你随某兴趣小组的同学一起来参加实验探究活动: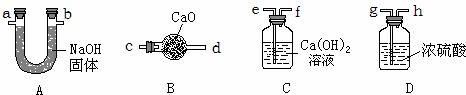
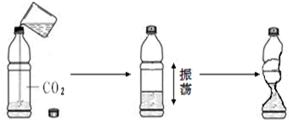


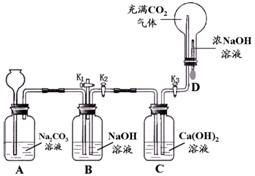 32、某化学兴趣小组设计了如图所示实验装置,进行了以下实验.
32、某化学兴趣小组设计了如图所示实验装置,进行了以下实验.