题目内容
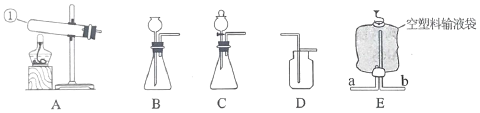
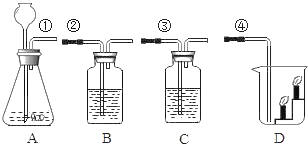
【题目】下图是实验室制取气体的常用装置:
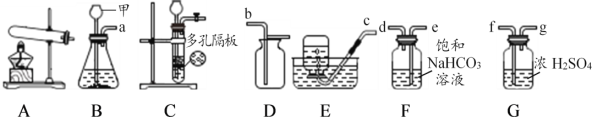
(1)仪器甲的名称是_____。
(2)若选A装置作为实验室制取氧气的发生装置,反应的化学方程式为:________;实验室可用B或C装置制取二氧化碳,选用C装置相对于B装置的优点是_________。
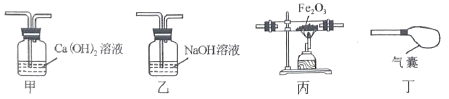
(3)实验室要制取纯净干燥的二氧化碳气体,装置接口连接顺序为:a→___→___→___→___→____(填接口对应的字母,全对才得分),F装置的作用_______。
【答案】长颈漏斗 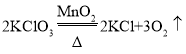 或
或 ![]() 控制反应的发生与停止 e d f g b 除去氯化氢气体
控制反应的发生与停止 e d f g b 除去氯化氢气体
【解析】
化学是一门以实验为基础的的自然科学。本题主要考查了常见仪器的用途、常见气体制备与收集装置的选择。选择何种装置制取气体,主要是由反应物状态和反应条件所决定的。收集气体的方法主要是由气体的密度及其在水中的溶解性等所决定的,是否与水反应等。
解:(1)仪器甲的名称是长颈漏斗;
(2)由装置A属于固固加热型,适用用氯酸钾或高锰酸钾制氧气,化学方程式为: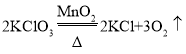 或
或![]() ;C装置配有多孔隔板和弹簧夹,可以实现固液分离,相对于B装置的优点是:能够控制反应的发生与停止;
;C装置配有多孔隔板和弹簧夹,可以实现固液分离,相对于B装置的优点是:能够控制反应的发生与停止;
(3)因为是用稀盐酸和石灰石(大理石)制取的二氧化碳,盐酸中的溶质是HCl,得到的二氧化碳可能含有少量的水蒸气和氯化氢气体,二氧化碳不和饱和的碳酸氢钠溶液反应而氯化氢气体能和饱和碳酸氢钠溶液反应,可用饱和碳酸氢钠溶液除去氯化氢气体,但依然会带有水份,再用浓硫酸除去水蒸气,多功能瓶洗气时长进短出,CO2密度比空气大且能溶于水,用向上排空气法收集,所以要得到纯净干燥的二氧化碳气体,装置接口连接顺序为:aedfgb。F是除去HCl气体。

 阅读快车系列答案
阅读快车系列答案【题目】某学校化学兴趣小组的同学们在实验室发现一瓶石灰水试剂瓶瓶壁和瓶塞周围有一些白色粉末。为了弄清楚白色粉末的成分及形成原因,他们进行了如下探究:
(提出问题)白色粉末成分的猜想和成因分析。
(做出猜想)①可能是CaCO3:原因是石灰水与空气中的CO2反应。
②可能是___________:原因是溶剂蒸发,石灰水中的溶质结晶析出。
③还可能是Ca(OH)2和CaCO3。
(实验探究)甲同学取白色粉末于试管中,加少量的水、振荡,发现试管底部有白色固体,于是他得出白色粉末是CaCO3的结论。乙同学认为甲同学的结论不严密,理由是______________________。
为了得出较严密的结论,他们进行了下表所示实验,请完成实验报告:
实验步骤 | 实验现象 | 实验结论 |
①取上述试管中的上层清液,滴加1~2滴无色酚酞试液 | 溶液呈红色 | 白色粉末中 ___________________ |
②往上述试管残留的白色固体中加入___________ | ___________ | 白色粉末中含有CaCO3 |
由上述实验可知,白色粉末成分的猜想③是正确的。
(拓展反思)通过上述实验的探究,同学们向实验员提出了保存、使用易变质溶液的下列建议,合理的是_________。
a 密封保存 b 使用前临时配制 c 禁止使用该试剂
【题目】2018年1月11日,广西某地高速公路大桥上用于融冰作业的2包共100公斤含有亚硝酸钠的工业盐遗失,当地迅速组织警力开展搜寻遗失的工业盐,确保不流入市场和家庭。
(资料卡1)亚硝酸钠与食盐氯化钠相似,为白色有咸味的固体,但误食会使人中毒。腌制食品、泡菜等制作过程中会产生亚硝酸钠。
根据以上资料,回答下列问题:
(1)用盐融冰的原理是____,该过程主要发生的是___(填“物理变化”或“化学变化”)。
(2)下图是用不同浓度盐水腌制泡菜过程中亚硝酸盐含量测定曲线图。据此回答:当盐水浓度为6%时,第____天亚硝酸盐含量达到最大值。为了安全,泡菜腌制时盐水浓度最好是____并在腌制____天后再食用。
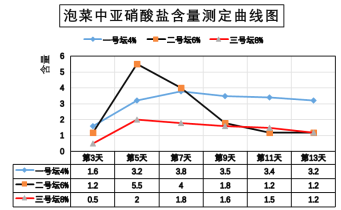
(3)兴趣小组欲测定某工业盐中亚硝酸钠的质量分数
(资料卡2)实验室常用亚硝酸钠与氯化铵溶液反应制取纯净的氮气,其化学方程式为:NaNO2 + NH4Cl ![]() NaCl + N2↑+ 2H2O(此反应是放热反应)
NaCl + N2↑+ 2H2O(此反应是放热反应)
(资料卡3)在酸性环境中高锰酸钾能与亚硝酸钠发生如下反应:2KMnO4 + 5NaNO2 + 3H2SO4 = K2SO4 + 2MnSO4 + 5NaNO3 + 3H2O
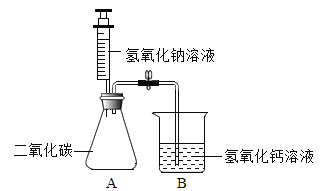
(方案一)取1g该工业盐样品与足量氯化铵溶液于如图装置中充分反应(该工业盐中其他成分不与氯化铵溶液反应),实验时加热片刻后,即可移去酒精灯,其原因___。最终量筒中收集到300mL水,已知该条件下氮气的密度为1.25g/L,则该工业盐样品中亚硝酸钠的质量分数为____(写出计算过程,结果保留一位小数,)。
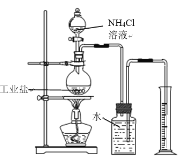
实验结束后发现测量结果偏大,可能原因是____。
(方案二)为更准确地测定该工业盐中亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用含量为15.8g/L的酸性KMnO4溶液进行反应,实验所得数据如下表所示:
实验次序 | 1 | 2 | 3 | 4 |
KMnO4溶液体积(mL) | 20.60 | 20.02 | 20.00 | 19.98 |
上述第____次实验所得数据明显异常,剔除异常数据后,计算出该工业盐中亚硝酸钠的质量分数为___。