题目内容
【题目】某同学在做实验时发现盛放NaOH溶液的试剂瓶口与橡皮塞上常有白色粉末出现,为探究这一白色粉末的成分,他做了以下实验:
(1)取少量白色粉末于试管中,再滴加稀HCl,有气泡产生,由此可推出白色粉末中含有 。
(2)该同学为进一步探究白色粉末是否含有NaOH,主要操作流程如下:
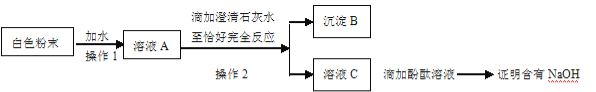
①沉淀B的化学式为 。
②在操作1中要用到玻璃棒,其作用是 ;在操作2中,除要用到铁架台(带铁圈)、烧杯、滤纸、玻璃棒外,还需补充的玻璃仪器是 。
③你认为该同学的这个方案是否正确? (填“正确”或“不正确”),
理由是
【答案】(1) Na2CO3;(2)①CaCO3,②加快溶解速率、漏斗,③不正确、石灰水和碳酸钠反应生成了氢氧化钠
【解析】
试题分析:(1)滴加稀HCl,有气泡产生,说明有碳酸盐,白色粉末中有碳酸钠;(2)①澄清石灰水溶质为氢氧化钙,和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以白色沉淀为碳酸钙,②在操作1中要用到玻璃棒,其作用是加快溶解速率,操作2为过滤,需要补充道额玻璃仪器为漏斗,③该方案不正确,碳酸钠和氢氧化钙反应生成氢氧化钠,会干扰实验。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目