题目内容
下表为氢氧化钙在不同温度下的溶解度。下列说法正确的是()
温度/°C | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
A.0°C时氢氧化钙的溶解度为0.19
B.氢氧化钙的溶解度随温度的升高而增大
C.将60°C时的氢氧化钙饱和溶液降温会析出晶体
D.40°C时,将0.15g氢氧化钙加入到100g水中充分溶解,得到溶液的质量为100.14g
我国著名化学家侯德榜先生发明的“侯氏制碱法”,因原料利用率高,能进行连续生产,从而享誉中外,如图为侯氏制碱法的基本流程示意图,回答问题。
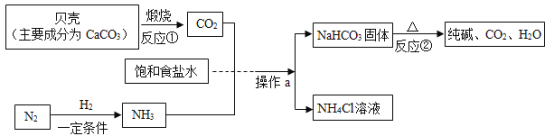
(1)操作a的名称是___________________________。
(2)反应②中的化学方程式为___________________________,其基本反应类型为___________________________。
(3)仔细观察流程图,其中可循环利用的物质是___________________________。
(4)化学肥料对农作物生长具有促进作用,得到的副产品NH4Cl属于___________________________(填字母)。
A 氮肥
B 磷肥
C 钾肥
D 复合肥
(5)该方法制出的纯碱固体中常含有NaCl,检验该固体中是否含有NaCl的方法是___________________________。
附:部分碱、酸、盐的溶解性表(20°C)
| OH- | NO3- | Cl- | CO32- |
H+ | 溶、挥 | 溶、挥 | 溶、挥 | |
Na+ | 溶 | 溶 | 溶 | 溶 |
Ag+ | 一 | 溶 | 不 | 不 |
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“挥”表示挥发性,“一”表示那种物质不存在或遇到水就分解了。
根据大量的实验总结,得出酸碱盐之间相互发生复分解反应的条件是生成物中有沉淀、气体或水。实验回顾如图:

请回答
(1)甲实验有沉淀生成:加入的试剂是_____;
(2)乙实验有气体生成:化学方程式_____,检验气体的方法为_____;
(3)丙实验有水生成:氢氧化钠溶液中加入酚酞的作用是_____;
(4)依据复分解反应的条件可判断硫酸和氯化镁溶液不能发生反应。若想确认两种物质没有发生复分解反应,需要检验溶液中存在_____(写微粒符号)。
提出新问题:我们已经知道能发生复分解反应的两种盐通常是可溶的。有没有某些可溶性盐和难溶性盐能发生复分解反应?
查阅资料:
难溶性盐 | AgI | AgCl |
20℃时在水中的溶解度 | 3×10‑7g | 1.5×10‑4g |
颜色 | 黄 | 白 |
(5)实验取证:取少量硝酸银溶液于试管中,滴加过量的氯化钠溶液,有白色沉淀产生,继续加入少量KI溶液,白色沉淀转化为黄色沉淀,加入少量KI溶液后发生反应的化学方程式_____;
(6)结论某些可溶性盐和难溶性盐之间能发生复分解反应。从微观角度分析原因:反应朝着溶液中离子浓度(单位体积溶液中离子数目的多少)_____(填“减少”或“增大”)的方向进行。



 加热时移走烧杯
加热时移走烧杯 加热试管内的液体
加热试管内的液体 倾倒液体
倾倒液体 收集氧气
收集氧气