题目内容
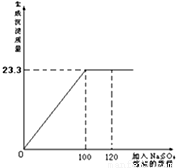
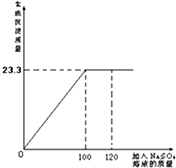 将24.1g由NaCl和BaCl2组成的固体混合物溶解于99.2mL水 中(P水=1g/cm3),向所得溶液中滴加质量分数为14.2%的Na2SO4溶液,至恰好完全反应.如图是所加Na2SO4溶液质量与生成沉淀质量的关系图,计算:
将24.1g由NaCl和BaCl2组成的固体混合物溶解于99.2mL水 中(P水=1g/cm3),向所得溶液中滴加质量分数为14.2%的Na2SO4溶液,至恰好完全反应.如图是所加Na2SO4溶液质量与生成沉淀质量的关系图,计算:
(1)生成沉淀的质量是多少?
(2)反应后所得溶液中溶质的质量分数为多少?
解:(1)由图可知,生成BaSO4沉淀的质量为23.3g.
(2)设BaCl2的质量x,生成NaCl的质量y
BaCl2+Na2SO4═BaSO4↓+2NaCl
208 233 117
x 23.3g y
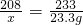
解之得 x=20.8g

解之得 y=11.7g
溶液的总质量=24.1g+99.2g+100g-23.3g=200g
溶质的总质量=11.7g+(24.1g-20.8g)=15g
溶质的质量分数=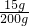 ×100%=7.5%
×100%=7.5%
答:(1)生成沉淀的质量是23.3g;(2)所得溶液中溶质的质量分数是7.5%.
分析:根据复分解反应发生的条件,混合物中NaCl和滴加的Na2SO4不能反应;根据关系图可知,混合物中的BaCl2和滴加的100gNa2SO4溶液交换成分恰好完全反应,生成23.3g的沉淀BaSO4.
(1)根据关系图,可读出恰好完全反应生成沉淀的量;
(2)恰好完全反应反所得溶液为NaCl溶液,其中溶质NaCl有两部分:一是原混合物中含有的NaCl,二是反应后生成的NaCl,计算溶质质量时要注意这点.
点评:反应后溶液的质量通常根据质量守恒进行计算,即反应后溶液质量=反应前所有物质的质量-生成的沉淀或气体质量-不参加反应的固体不溶物质量.
(2)设BaCl2的质量x,生成NaCl的质量y
BaCl2+Na2SO4═BaSO4↓+2NaCl
208 233 117
x 23.3g y
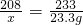
解之得 x=20.8g

解之得 y=11.7g
溶液的总质量=24.1g+99.2g+100g-23.3g=200g
溶质的总质量=11.7g+(24.1g-20.8g)=15g
溶质的质量分数=
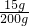 ×100%=7.5%
×100%=7.5%答:(1)生成沉淀的质量是23.3g;(2)所得溶液中溶质的质量分数是7.5%.
分析:根据复分解反应发生的条件,混合物中NaCl和滴加的Na2SO4不能反应;根据关系图可知,混合物中的BaCl2和滴加的100gNa2SO4溶液交换成分恰好完全反应,生成23.3g的沉淀BaSO4.
(1)根据关系图,可读出恰好完全反应生成沉淀的量;
(2)恰好完全反应反所得溶液为NaCl溶液,其中溶质NaCl有两部分:一是原混合物中含有的NaCl,二是反应后生成的NaCl,计算溶质质量时要注意这点.
点评:反应后溶液的质量通常根据质量守恒进行计算,即反应后溶液质量=反应前所有物质的质量-生成的沉淀或气体质量-不参加反应的固体不溶物质量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
NaNO2(亚硝酸钠)、NaCl和物质M (不含结晶水)的溶解度曲线如图24-1所示,请根据图像和有关信息回答下列问题:
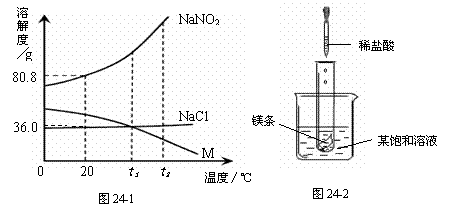 |
(1)t2 ℃时,NaNO2、NaCl和M的溶解度由大到小的顺序是 。
(2)如图24-2所示,当往试管中加入5mL稀盐酸时,试管内立刻产生大量气泡,同时放热使烧杯中饱和溶液变浑浊(不考虑水分蒸发)。请判断:该饱和溶液中的溶质是NaNO2、NaCl和M中的 。
(3)分别将NaNO2、NaCl和M的饱和溶液从t2℃降温到t1℃时,三种溶液中溶质的质量分数由大到小的顺序是 。
(4)NaNO2有毒,其外观和咸味与食盐很相似,因此要防止因误食NaNO2而发生中毒事故。为了区别NaNO2、NaCl固体,某化学兴趣小组同学查阅资料获得如下信息: NaNO2的水溶液呈碱性,NaCl的水溶液呈中性;NaNO2熔点为271 ℃,NaCl熔点为801 ℃。
① 小明同学设计的鉴别实验方案如下:
20℃时分别取NaNO2、NaCl各5.0g于两只小烧杯中,分别加入10mL水(水的密度近似看作1g/cm3),用玻璃棒充分搅拌后观察。你认为此方案是否可行 (填“可行”或“不可行”)。
② 该小组其他同学又设计出与小明不同的实验方案,并获得成功。你认为该方案可能是 (只填写一种方案并简单叙述)。
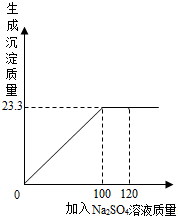 (2012?乐山三模)将24.1g由NaCl和BaCl2组成的固体混合物溶解于99.2mL水 中(P水=1g/cm3),向所得溶液中滴加质量分数为14.2%的Na2SO4溶液,至恰好完全反应.如图是所加Na2SO4溶液质量与生成沉淀质量的关系图,计算:
(2012?乐山三模)将24.1g由NaCl和BaCl2组成的固体混合物溶解于99.2mL水 中(P水=1g/cm3),向所得溶液中滴加质量分数为14.2%的Na2SO4溶液,至恰好完全反应.如图是所加Na2SO4溶液质量与生成沉淀质量的关系图,计算: