题目内容
把镁和铜的混合物20g和足量稀硫酸反应,生成氢气0.4g,求原混合物中铜的质量.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:镁会和盐酸反应;但是铜不会和盐酸反应;写出化学方程式并代入氢气的质量计算出镁的质量,然后计算铜的质量.
解答:解:设混合物里含镁的质量为x.
Mg+H2SO4=MgSO4+H2↑
24 2
x 0.4g
=
x=4.8g
∴铜的质量=20g-4.8g=15.2g
答案:原混合物中铜的质量15.2g
Mg+H2SO4=MgSO4+H2↑
24 2
x 0.4g
| 24 |
| 2 |
| x |
| 0.4g |
x=4.8g
∴铜的质量=20g-4.8g=15.2g
答案:原混合物中铜的质量15.2g
点评:掌握化学方程式的计算格式和规范性,注意:镁会和硫酸反应;但是铜不会和硫酸反应.

练习册系列答案
相关题目
如图为初中化学常见气体的发生装置与收集装置,有关这些装置的说法不正确的是( )
A、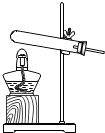 如图装置可作为加热固体制取气体的发生装置 |
B、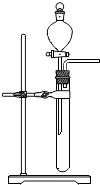 如图装置中分液漏斗的作用是方便添加液体药品 |
C、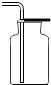 如图装置可用于收集H2、CO2 |
D、 如图装置可用于收集H2、O2 |

 某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,蜡烛燃烧却有明亮的火焰,该小组同学进行了如下探究.
某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,蜡烛燃烧却有明亮的火焰,该小组同学进行了如下探究.
