题目内容
(2013?天桥区二模)为测定某化肥[(NH4)2SO4和NH4Cl组成]的含氮量,取12g于研钵中,向其中加入氢氧化钙充分反应,当加入7.4g氢氧化钙时恰好完全反应,则此化肥中氮元素的质量分数约为( )
分析:根据[(NH4)2SO4和NH4Cl与氢氧化钙反应的方程式,找出氢氧化钙与生成的氨气的关系式,由氢氧化钙的质量求出氨气质量,再求出氮元素质量,由元素质量守恒可知化肥中的氮元素的质量,即可求出此化肥中氮元素的质量分数
解答:解:设生成氨气的质量为x
由Ca(OH)2+(NH4)2SO4═CaSO4+2NH3↑+2H2O
2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑
得:Ca(OH)2~2NH3
74 34
7.4g x
=
解得:x=3.4g
此化肥中氮元素的质量分数约为:
×100%=23.3%
由以上计算可知,B正确,A、C、D错误.
故选B.
由Ca(OH)2+(NH4)2SO4═CaSO4+2NH3↑+2H2O
2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑
得:Ca(OH)2~2NH3
74 34
7.4g x
| 74 |
| 34 |
| 7.4g |
| x |
此化肥中氮元素的质量分数约为:
3.4g×
| ||
| 12g |
由以上计算可知,B正确,A、C、D错误.
故选B.
点评:在解答本题时,利用元素守恒能求出氨气中氮元素的质量,就可以计算出此化肥中氮元素的质量分数.

练习册系列答案
相关题目
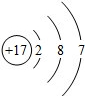 (2013?天桥区二模)如图所示为某原子的结构示意图,下列有关说法错误的是( )
(2013?天桥区二模)如图所示为某原子的结构示意图,下列有关说法错误的是( )