题目内容
(2013?明溪县质检)下列依据实验目的所设计的实验操作中,正确的是( )
分析:A、检验NaCl中含有Na2CO3,主要根据碳酸钠和氯化钠的性质不同来选用合适的试剂;
B、要鉴别氢氧化钙和氢氧化钠,所选试剂与这两种溶液混合需有明显的不同现象;
C、盐酸不仅能和杂质碳酸钙反应,而且能够和主要成分氧化钙反应;
D、根据CO2和CO的性质判断,二氧化碳能和碱溶液反应.
B、要鉴别氢氧化钙和氢氧化钠,所选试剂与这两种溶液混合需有明显的不同现象;
C、盐酸不仅能和杂质碳酸钙反应,而且能够和主要成分氧化钙反应;
D、根据CO2和CO的性质判断,二氧化碳能和碱溶液反应.
解答:解:A、氯化钠和碳酸钠都易溶于水,加水溶解无法检验NaCl中是否含有Na2CO3,故A错误;
B、碳酸钠溶液与氢氧化钙混合产生白色沉淀,与氢氧化钠溶液混合不反应,可以鉴别,故B正确;
C、盐酸不仅能和杂质碳酸钙反应,而且能够和主要成分氧化钙反应,故C错误;
D、将气体通入足量NaOH溶液中,二氧化碳能和氢氧化钠反应被吸收,一氧化碳不反应,因此除去的是二氧化碳,故D错误.
故选B.
B、碳酸钠溶液与氢氧化钙混合产生白色沉淀,与氢氧化钠溶液混合不反应,可以鉴别,故B正确;
C、盐酸不仅能和杂质碳酸钙反应,而且能够和主要成分氧化钙反应,故C错误;
D、将气体通入足量NaOH溶液中,二氧化碳能和氢氧化钠反应被吸收,一氧化碳不反应,因此除去的是二氧化碳,故D错误.
故选B.
点评:进行物质鉴别时,根据物质的不同性质,采用物理或化学的方法加以鉴别,所选的鉴别试剂与物质混合时,应有明显的不同的现象;除杂质的原则:首先方法要可行,既要能除掉杂质,又不能和需要的物质反应,同时也不能添加新的杂质,另外,实验操作越简单越好.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案
相关题目
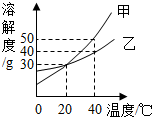 (2013?明溪县质检)甲、乙两种固体物质的溶解度曲线如图所示.
(2013?明溪县质检)甲、乙两种固体物质的溶解度曲线如图所示.