题目内容
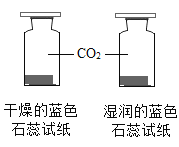
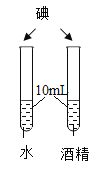
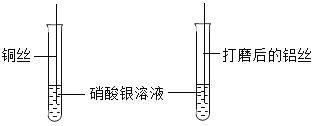
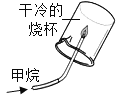
【题目】化学小组为探究铝、铜、银三种金属的活动性顺序,设计了如图所示实验方案。下列说法中不正确的是
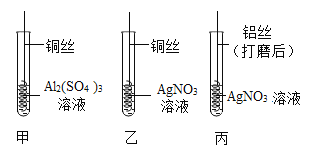
A.由实验乙可得出金属活动性:Cu>Ag
B.只由实验甲、乙可得出金属活动性:Al>Cu>Ag
C.只由实验甲、丙可得出金属活动性:Al>Cu>Ag
D.实验甲中的Al(SO4)3溶液改为Al(NO3)3溶液也能完成实验
【答案】C
【解析】
A、实验乙中,铜丝可以与硝酸银发生置换反应,析出银单质,可得出金属活动性:Cu>Ag;故选项正确,但不符合题意;
B、实验甲中铜丝不能与硫酸铝反应,则说明金属活动性:铝>铜;实验乙中铜丝可以与硝酸银发生置换反应,析出银单质,说明金属活动性:铜>银,整理可得出金属活动性:Al>Cu>Ag;故选项正确,但不符合题意;
C、实验甲中铜丝不能与硫酸铝反应,则说明金属活动性:铝>铜;实验丙中铝可以与硝酸银发生置换反应,析出银单质,则说明金属活动性:铝>银;不能比较铜和银的金属活动性强弱关系;故选项错误,但符合题;
D、实验甲中的Al(SO4)3溶液改为Al(NO3)3溶液,铜丝不能与硝酸铝反应,则说明金属活动性:铝>铜;也能完成实验;故选项正确,但不符合题意;
故选:C。

 每日10分钟口算心算速算天天练系列答案
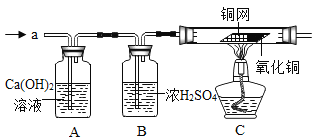
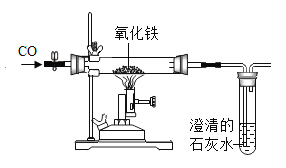
每日10分钟口算心算速算天天练系列答案【题目】某小组在实验室利用如下装置进行实验:I.CO还原Fe2O3;II.探究产物成分。
I.CO还原Fe2O3
(1)检查装置气密性、添加药品、连接装置,接下来的操作是__________(填序号);
a.先通一氧化碳;b.先点燃酒精喷灯加热
(2)写出该条件下CO还原Fe2O3的化学方程式:___________。
(3)上图装置中不足之处是_________。
II.探究产物成分
(4)对黑色产物的成分进行探究:
①经查阅资料可知,在不同温度下,该还原反应的过程如下:
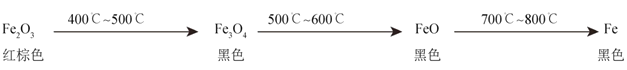
②已知Fe3O4、FeO 与稀盐酸反应不会产生气泡,与CuSO4溶液不反应。
提出问题:反应后所得黑色固体的成分?
提出猜想:关于黑色固体组成有很多种可能,现针对其中三种合理猜想进行探究
①Fe3O4和FeO
②_____和______(写化学式)
③Fe .
实验验证过程如下:
操作 | 反应现象 | 化学方程式 |
步骤1:取少量黑色固体于试管中,滴加足量稀盐酸,振荡。 | 固体:黑色固体完全消失; 液体:由无色变为浅绿色; 气体:有气泡产生。 | _________, |
步骤2:取少量黑色固体于试管中,滴加足量CuSO4溶液,振荡。 | 固体: 黑色固体完全消失,________, 液体:______。 | Fe+CuSO4=Cu+FeSO4 |
得出结论:猜想_____________________是正确的(选填“①”或“②”或“③”);
(5)称重分析:由以上实验可知,若有纯净Fe2O3 (相对分子质量为160) 样品16g, 通入CO完全反应(到固体质量不再减少),剩余固体质量为_________g。