题目内容
 某校九年级综合实践活动小组为探究鸡蛋壳的成份中含有多少碳酸钙,称取10g的鸡蛋壳,用足量的稀盐酸与之充分反应后,得到一种能使澄清石灰水变浑浊的无色气体,最后所得气体质量与反应时间的关系如图所示.则:
某校九年级综合实践活动小组为探究鸡蛋壳的成份中含有多少碳酸钙,称取10g的鸡蛋壳,用足量的稀盐酸与之充分反应后,得到一种能使澄清石灰水变浑浊的无色气体,最后所得气体质量与反应时间的关系如图所示.则:
(1)待反应结束时,共产生______g______气体;
(2)试计算10g鸡蛋壳中碳酸钙的质量.
解:(1)鸡蛋壳的主要成分为碳酸钙,所以加入盐酸后生成的气体为二氧化碳,根据坐标系可以知道生成二氧化碳气体的质量为2.2g;
(2)设10g鸡蛋壳中碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2g
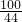 =
=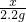
解得:x=5g;
答:10g鸡蛋壳中碳酸钙的质量为5g.
故答案为:(1)2.2;二氧化碳;
(2)5g.
分析:(1)根据题干可以知道所发生的反应为碳酸钙和盐酸的反应,生成的气体为二氧化碳,可以据此作答;
(2)根据坐标系中所给气体的质量结合化学方程式可以求算出碳酸钙的质量.
点评:利用化学方程式计算,首先必须读懂题意,然后根据化学方程式的计算步骤进行.注意的要点有:正确地写出反应的化学方程式、相对分子质量的计算不要马虎、化学方程式中任意两种物质之间都存在固定的比例关系,解题的过程要规范.
(2)设10g鸡蛋壳中碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2g
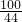 =
=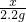
解得:x=5g;
答:10g鸡蛋壳中碳酸钙的质量为5g.
故答案为:(1)2.2;二氧化碳;
(2)5g.
分析:(1)根据题干可以知道所发生的反应为碳酸钙和盐酸的反应,生成的气体为二氧化碳,可以据此作答;
(2)根据坐标系中所给气体的质量结合化学方程式可以求算出碳酸钙的质量.
点评:利用化学方程式计算,首先必须读懂题意,然后根据化学方程式的计算步骤进行.注意的要点有:正确地写出反应的化学方程式、相对分子质量的计算不要马虎、化学方程式中任意两种物质之间都存在固定的比例关系,解题的过程要规范.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
 某校九年级综合实践活动小组用某种过氧化氢溶液和二氧化锰来制取氧气,反应结束后所得气体质量与时间的关系如图所示.请计算:所用溶液中含过氧化氢的质量?(要求写出解题过程)
某校九年级综合实践活动小组用某种过氧化氢溶液和二氧化锰来制取氧气,反应结束后所得气体质量与时间的关系如图所示.请计算:所用溶液中含过氧化氢的质量?(要求写出解题过程) 某校九年级综合实践活动小组为探究鸡蛋壳的成份中含有多少碳酸钙,称取10g的鸡蛋壳,用足量的稀盐酸与之充分反应后,得到一种能使澄清石灰水变浑浊的无色气体,最后所得气体质量与反应时间的关系如图所示.则:
某校九年级综合实践活动小组为探究鸡蛋壳的成份中含有多少碳酸钙,称取10g的鸡蛋壳,用足量的稀盐酸与之充分反应后,得到一种能使澄清石灰水变浑浊的无色气体,最后所得气体质量与反应时间的关系如图所示.则: 为了研究炼铁原理,某校九年级综合实践活动小组按图所示,用一氧化碳与氧化铁反应进行实验,现请你一起参与.
为了研究炼铁原理,某校九年级综合实践活动小组按图所示,用一氧化碳与氧化铁反应进行实验,现请你一起参与.