题目内容
【题目】(5 分)下图是元素周期表的一部分,请回答相关问题:
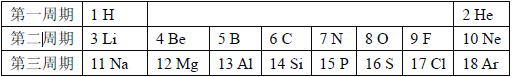
(1)氟元素与氯元素位于同一纵行的原因是 ,它们在化学反应中都易 (填“得到”或“失去”)电子,铝元素与氯元素形成化合物的化学式是 。
(2)M2—与Ne 核外电子排布相同,则M 元素的名称为 。已知M 元素的相对原子质量为a,则M 元素原子核内的中子数为 。
【答案】(1)最外层电子数相同,得到,AlCl3 (2)氧元素,a-8
【解析】
试题分析:(1)同一纵行的元素原子的最外层电子数相同,氟元素与氯元素的最外层电子数为7;它们的最外层大于4,易得到电子形成稳定结构;铝元素显+3价,氯元素为-1价根据化合物的化学式的写法:正价在左,负价在右,正负化合价代数和为0的原则,可知氯化铝的化学式为AlCl3;
(2)Ne 核外电子排布为2、8,)M2—带两个单位的负电荷,即得到了两个电子,那么M原子的核外电子数为8,即质子数为8,故M是氧元素;相对原子质量=质子数+中子数,故M 元素原子核内的中子数=相对原子质量-质子数=a-8 。

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目