题目内容
【题目】小明用传感器探究稀氢氧化钠溶液与稀盐酸反应过程中温度和pH的变化。测定结果如图所示。根据图示回答下列问题:
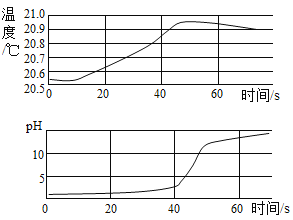
(1)氢氧化钠和盐酸的反应属于_______(填“吸热”或“放热”)反应。
(2)写出61s时,溶液中溶质的化学式____________。
【答案】放热 ![]()
【解析】
图象中pH值的变化是从小于7逐渐的增大到大于7,则原溶液显酸性,不断的加入碱性溶液,则是将稀氢氧化钠溶液滴加到稀盐酸中。
(1)由图象可知,向稀盐酸中滴加氢氧化钠溶液时,溶液的温度在升高,说明氢氧化钠和盐酸反应属于放热反应。
(2)61s时,溶性显碱性,则是氢氧化钠溶液过量,稀盐酸消耗完,溶液中溶质是稀盐酸和氢氧化钠生成的氯化钠和过量的氢氧化钠,化学式为![]() 。
。

练习册系列答案
相关题目
【题目】下表为氯化铵和氯化钠在不同温度时的溶解度,回答下列问题:
温度/°C | 0 | 10 | 20 | 30 | 40 | 50 |
NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(1)由表中数据可知,溶解度随温度变化较大的物质是____________。
(2)20°C时75g水中最多只能溶解NaCl__________g;氯化钠与氯化铵溶解度相等的温度在_________°C之间。
(3)向烧杯中加入100g水和50. 0g氯化铵配制成50°C的溶液,再冷却到30°C ,烧杯中析出固体的质量为___________g。