题目内容
24、已知Fe+CuSO4=Cu+FeSO4.将足量的细铁丝放入一定量的硫酸铜溶液中,则下列图形表示正确的是( )
分析:先对方程式进行分析,由Fe+CuSO4=Cu+FeSO4可以看出每反应56份的铁则会生成64份的铜,固体质量在不断增加,再结合实际判断即可.
解答:解:
由方程式Fe+CuSO4=Cu+FeSO4可以看出,在发生置换反应时固体质量会不断地增加,直至硫酸铜被耗尽,固体质量不再变化,因此固体质量的曲线应该先上升,而后形成一条直线,且反应开始固体质量是铁丝的质量,所以质量不能是0.
故选B
由方程式Fe+CuSO4=Cu+FeSO4可以看出,在发生置换反应时固体质量会不断地增加,直至硫酸铜被耗尽,固体质量不再变化,因此固体质量的曲线应该先上升,而后形成一条直线,且反应开始固体质量是铁丝的质量,所以质量不能是0.
故选B
点评:此题是对Fe+CuSO4=Cu+FeSO4这一反应的探讨,解题的关键是能够判断该反应进行时固体质量增加的事实.

练习册系列答案
相关题目
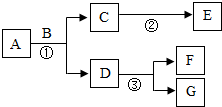
 已知Fe+CuSO4═Cu+FeSO4,A~G是初中化学常见的7种物质,其中至少有一种物质是无色气体,且A与G含有相同的金属元素.它们在一定条件下转化关系如图所示,其中部分反应物或生成物已略去.回答问题:若A中两种元素的质量比为7:3,F是一种红色金属,则F的化学式为
已知Fe+CuSO4═Cu+FeSO4,A~G是初中化学常见的7种物质,其中至少有一种物质是无色气体,且A与G含有相同的金属元素.它们在一定条件下转化关系如图所示,其中部分反应物或生成物已略去.回答问题:若A中两种元素的质量比为7:3,F是一种红色金属,则F的化学式为