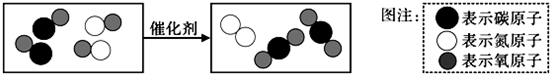
题目内容
(7分)铁在潮湿的空气中容易生锈。
(1)防止铁生锈的措施有 (写一点即可),其原理是__________。
(2)铁锈的主要成分是________,将一生锈的铁钉放入稀盐酸中除锈,观察到的现象是溶液变为__________色,同时看到有气泡冒出,写出发生反应的化学方程式:___________________、____________________。
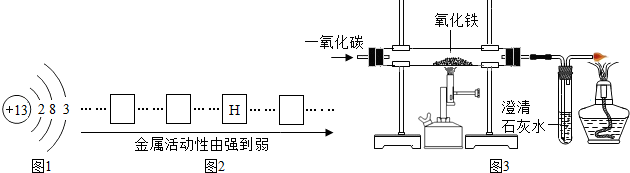
(3)回收再利用生锈的铁制品是保护金属资源的一种有效途径。右图所示的废铁粉中Fe2O3含量大约在80%
(其余20%为铁)左右,回收后在工业上常用一氧化碳将其还原,反应的化学方程式是_______________。
(1)刷漆 隔绝空气和水 (合理即给分)
(2)Fe2O3 黄 Fe2O3 + 6HCl ="=" 2FeCl3 + 3H2O Fe + 2HCl ="=" FeCl2 + H2↑ (3)3CO + Fe2O3 2Fe + 3CO2
(3)3CO + Fe2O3 2Fe + 3CO2
解析试题分析:(1)铁生锈的原理是铁与空气中的氧气和水共同作用的结果,故可使金属与水和氧气隔绝就可以防止生锈,如刷油漆可以防止铁生锈,其原理就是隔绝空气和水。
(2)铁锈的主要成分是氧化铁,氧化铁能和稀盐酸反应生成氯化铁(黄色溶液)和水,即Fe2O3+6HCl═2FeCl3+3H2O,故可观察到的现象是溶液变为黄色;继而铁能和稀盐酸反应生成氯化亚铁(浅绿色溶液)和氢气,即Fe+2HCl═FeCl2+H2↑,故可见气泡冒出。
(3)氧化铁和一氧化碳在高温条件下反应能生成铁和二氧化碳,故反应的化学方程式为3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
考点:金属锈蚀的条件及其防护,一氧化碳还原氧化铁,铁锈的主要成分,金属的回收利用及其重要性,书写化学方程式
点评:本题主要考查金属生锈的条件、防止生锈的方法及其化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律。