题目内容
以下除杂质的方法(括号内物质为杂质)正确的是
| A.CaO(CaCO3),加适量稀盐酸 |
| B.Ca(OH)2(NaOH),加入适量碳酸钠溶液后过滤 |
| C.HNO3(HCl),加适量的硝酸银溶液后过滤 |
| D.CO2(CO),在足量的氧气中点燃 |
C
A.CaO(CaCO3),加适量稀盐酸,也将氧化钙除去了,不正确; B.Ca(OH)2(NaOH),加入适量碳酸钠溶液后过滤,没将杂质除去,却将氢氧化钙除去了,不合理;C.HNO3(HCl),加适量的硝酸银溶液后过滤,可以达到目的;正确; D.CO2(CO),在足量的氧气中点燃,少量的一氧化碳在二氧化碳中不易点燃,错误;
故答案为C。
故答案为C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
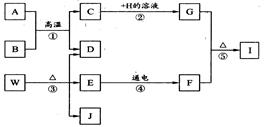
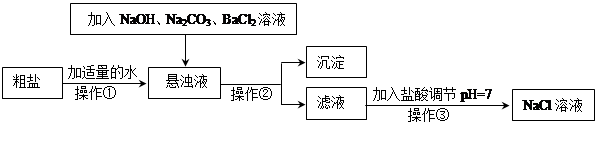 回答下列问题:
回答下列问题: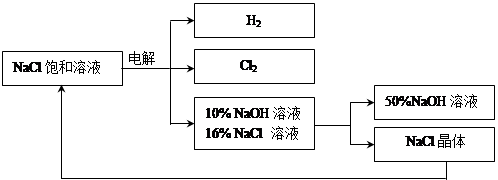
 Cl2 ↑+ H2 ↑ + 2NaOH,电解后溶液的pH 。(填“升高”、“不变”、“降低”)
Cl2 ↑+ H2 ↑ + 2NaOH,电解后溶液的pH 。(填“升高”、“不变”、“降低”)