题目内容
根据金属活动性顺序的相关知识,回答下列问题.(1)将某金属M加入稀硫酸中,观察到金属M表面有气泡产生,M在金属活动性顺序表中的位置是在氢的 .
(2)在相同条件下,把金属M及另外三种金属分别加入同浓度、等体积的稀硫酸中,观察反应产生气泡的剧烈程度,并记录如下(反应剧烈程度用“+”的多少表示):
| 金属 | 金属1 | 金属2 | 金属M | 金属3 |
| 反应剧烈程度 | ++++ | +++ | ++ | + |
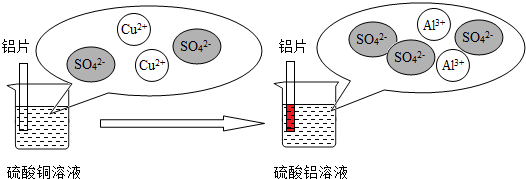
(3)铝和硫酸铜溶液反应的过程如下图所示:
上述反应的化学方程式是 ,从微观粒子变化的角度分析铝片在硫酸铜溶液中发生的变化 .
(4)向硝酸银和硝酸铜的混合液中加入一些镁粉,充分反应后过滤.若向滤渣中滴加稀盐酸后没有气泡产生,则下列说法正确的是 (填字母序号).
A.滤渣中可能含有铜,滤液中一定含有硝酸镁
B.滤渣中可能含有银,滤液中一定没有硝酸铜
C.滤渣中可能含有镁,滤液中可能含有硝酸银
D.滤渣中一定含有银,滤液中可能含有硝酸银

【答案】分析:(1)根据金属活动顺序的应用,M能置换出氢,说明其活动性在H前面.
(2)可根据金属活动性顺序回答,金属越活泼,与酸反应越剧烈.
(3)铝的金属性比铜强,铝能与硫酸铜反应
(4)根据金属活动顺序的应用,排在前面的金属能把后面的金属从其盐溶液中置换出来来解答.
解答:解:(1)将某金属M加入稀硫酸中,观察到金属M表面有气泡产生,说明M能与酸反应放出氢气,故M的活动性比H强,排在氢的前面.
(2)Al,Mg,Fe,Zn的活动性顺序为Mg,Al,Zn,Fe,故M为Zn.
(3)铝的金属性比铜强,故铝能与硫酸铜反应,铝与硫酸铜反应的本质观察下图可知:铝原子失电子变成铝离子,铜离子得电子变成铜原子;
(4)镁的活动性比银和铜强,铜又比银强,在反应中镁会先置换活动性弱的银,然后再置换出铜,则被置换出的金属中一定含有银,可能含有铜;滤液中一定含有硝酸镁.可能含有硝酸银也可能含有硝酸铜;
故答案为:(1)前面.
(2)Zn
(3)2Al+3CuSO4=Al2(SO4)3+3Cu;铝原子失电子变成铝离子,铜离子得电子变成铜原子
(4)AD
点评:本题从多方位考查了金属的活动性,充分运用了金属活动性顺序,对提高同学们的分析能力很有帮助.
(2)可根据金属活动性顺序回答,金属越活泼,与酸反应越剧烈.
(3)铝的金属性比铜强,铝能与硫酸铜反应
(4)根据金属活动顺序的应用,排在前面的金属能把后面的金属从其盐溶液中置换出来来解答.
解答:解:(1)将某金属M加入稀硫酸中,观察到金属M表面有气泡产生,说明M能与酸反应放出氢气,故M的活动性比H强,排在氢的前面.
(2)Al,Mg,Fe,Zn的活动性顺序为Mg,Al,Zn,Fe,故M为Zn.
(3)铝的金属性比铜强,故铝能与硫酸铜反应,铝与硫酸铜反应的本质观察下图可知:铝原子失电子变成铝离子,铜离子得电子变成铜原子;
(4)镁的活动性比银和铜强,铜又比银强,在反应中镁会先置换活动性弱的银,然后再置换出铜,则被置换出的金属中一定含有银,可能含有铜;滤液中一定含有硝酸镁.可能含有硝酸银也可能含有硝酸铜;
故答案为:(1)前面.
(2)Zn
(3)2Al+3CuSO4=Al2(SO4)3+3Cu;铝原子失电子变成铝离子,铜离子得电子变成铜原子
(4)AD
点评:本题从多方位考查了金属的活动性,充分运用了金属活动性顺序,对提高同学们的分析能力很有帮助.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
根据金属活动性顺序的相关知识,回答下列问题.
(1)将某金属M加入稀硫酸中,观察到金属M表面有气泡产生,M在金属活动性顺序表中的位置是在氢的________.
(2)在相同条件下,把金属M及另外三种金属分别加入同浓度、等体积的稀硫酸中,观察反应产生气泡的剧烈程度,并记录如下(反应剧烈程度用“+”的多少表示):
| 金属 | 金属1 | 金属2 | 金属M | 金属3 |
| 反应剧烈程度 | ++++ | +++ | ++ | + |
(3)铝和硫酸铜溶液反应的过程如下图所示:
上述反应的化学方程式是________,从微观粒子变化的角度分析铝片在硫酸铜溶液中发生的变化________.
(4)向硝酸银和硝酸铜的混合液中加入一些镁粉,充分反应后过滤.若向滤渣中滴加稀盐酸后没有气泡产生,则下列说法正确的是________(填字母序号).
A.滤渣中可能含有铜,滤液中一定含有硝酸镁
B.滤渣中可能含有银,滤液中一定没有硝酸铜
C.滤渣中可能含有镁,滤液中可能含有硝酸银
D.滤渣中一定含有银,滤液中可能含有硝酸银